(单词翻译:单击)
得分 | 评卷人 |
一、选择(选出下列各题中惟一正确的答案。1—11题每题2分,12—13题每题3分,共28分。不选、多选、错选不得分)
1.下列日常生活中发生的变化,都属于化学变化的一组是 ( )
A.汽油挥发、铁铸成锅 B.水受热沸腾、酒精燃烧
C.瓷碗破碎、钢铁生锈 D.食物腐败、动植物呼吸
2.下列关于水的认识正确的是 ( )
A.水是常用的溶剂,许多物质都能溶于水
B.水体有自净能力,生活污水可任意排放
C.为了节约用水,提倡用工业废水直接灌溉农田
D.用沉淀、过滤和蒸馏等方法净化水,效果最好的是过滤
3.与元素的化学性质关系最密切的是 ( )
A.元素的核电荷数 B.原子的最外层电子数
C.原子的核外电子数 D.元素 的相对原子质量
的相对原子质量
4.下列变化能证明分子可以再分的是 ( )
A.水蒸发 B.石蜡熔化 C.干冰升华 D.水通电分解
5.食盐是重要的调味品,精盐是由粗盐提纯而来,在提纯过程中通常不需要的操作是( )
A.吸附 B.蒸发 C.过滤 D.溶解
6.农作物在缺氮的情况下,生长迟缓、叶色发黄。这时需施用的化肥是 ( )
A.KCl B.NH4HCO3 C.K2SO4 D.Ca(H2PO4)2
7.正确操作是实验安全、成功的关键。下列说法不正确的是 ( )
A.禁止向燃着的酒精灯内添加酒精
B.加热试管里的液体,试管外壁应干燥
C.可以用手触摸药品
D.用托盘天平称量,左盘放称量物,右盘放砝码
8.分类法是学习化学的有效方法之一。下列各组物质按照混合物、氧化物、单质的顺序排列的是 ( )
A.空气、水、氧气 B.氮气、氯酸钾、钢
C.石油、熟石灰、石墨 D.冰水混合物、纯碱、干冰
9.洗涤与生活密切相关。下列洗涤方法中利用 了乳化原理的是 ( )
了乳化原理的是 ( )
A.用盐酸清洗水垢 B.用洗洁精清洗餐具
C.用汽油洗涤油污 D.用酒精洗去试管中的碘
10.下列关于碳与碳的氧化物的说法不正确的是 ( )
A.木炭和一氧化碳都具有还原性
B.金刚石、石墨和C60都是碳元素的单质
C.二氧化碳能使被石蕊染成紫色的干花变红
D.在一定条件下二氧化碳能转化为一氧化碳
11.将50℃的硝酸钠饱和 溶液降温到20℃,有晶体析出(晶体中不含水)。下列有关量中没有发生改变的是 ( )
溶液降温到20℃,有晶体析出(晶体中不含水)。下列有关量中没有发生改变的是 ( )
A.硝酸钠的溶解度 B.溶液中溶质的质量
C.溶液中溶剂的质量 D.溶液中溶质的质量分数
12.下列实验用品:①pH试纸②无色酚酞溶液③紫色石蕊溶液④碳酸钠溶液,其中能将稀硫酸、氯化钠溶液和澄清石灰水鉴别出来的是 ( )
A.①②③ B.①③④ C.②③④ D.①②④
13.聪聪同学查阅资料获得有关物质燃烧的新信息:
⑴2Mg+CO2 2MgO+C ⑵H2+Cl2
2MgO+C ⑵H2+Cl2 2HCl
2HCl
由此形成以下几点认识:
①反应⑴属于置换反应 ②施用二氧化碳灭火也应有所选择 ③燃烧不一定要有氧气参加,其中正确的是 ( )
A.只有①② B.只有①③ C.只有②③ D.①②③
得分 | 评卷人 |
二、填空(共14分)
14.(4分)正确运用化学用语是学好 化学的基础。请用化学符号完成下表中的空格。
化学的基础。请用化学符号完成下表中的空格。

15.(4分)科学家发现海底埋藏着大量的“可燃冰”,其中主要含有甲烷水合物。甲烷中各元素的质量比是__________,甲烷燃烧的化学方程式为__________。“可燃冰”将成为未来新能源,但目前在开采技术上还存在困 难。开采中甲烷气体一旦泄露可能导致的后果是__________。
难。开采中甲烷气体一旦泄露可能导致的后果是__________。
16.(6分)氢氧化钾是一种重要的化工原料。将贝壳(主要成分是碳酸钙)灼烧后的固体与草木灰(主 要成分是碳酸钾)在水中相互作用,也可生成氢氧化钾。
要成分是碳酸钾)在水中相互作用,也可生成氢氧化钾。
⑴上述过程中发生反应的基本类型共有__________种。
⑵发生复分解反应的 化学方程式为__________。
化学方程式为__________。
⑶如果要得到氢氧化钾溶液,还要经过__________操作。
得分 | 评卷人 |
三、应用(共15分)
17.(9分)硫酸和盐酸是实验室常用的试剂,它们具有相似的化学性质。小华同学在复习有关酸的化学性质时,归纳出一下几点,但并不完 整,请你喝他一起完成。
整,请你喝他一起完成。
⑴
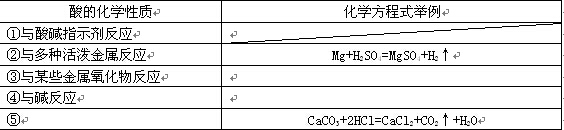
⑵生活中的食醋含有醋酸,用铁锅炒菜时放点食醋,可补充人体需要的微量元素__________,该反应的原理体现了酸的化学性质__________(填序号)。根据酸的化学性质,再举一例食醋在生活中的应用 _________ 。
⑶盐酸、硫酸、醋酸具有相似的化学性质时应为它们的水溶液中都含有__________。
18.(6分)将黄铜(铜锌合金)粉末20g与足量稀硫酸反应,得到0.2g氢气。
⑴计算这种合金中铜的质量分数。
⑵将黄铜片和纯铜片互相刻画,纯铜片上留有刻痕,说明 __________。
得分 | 评卷人 |
四、实验探究(共18分)
19.(9分)图A、B是实验室制气体的常用装置。


⑴写出装置B中有标号的仪器名称:a __________;b__________。
⑵如用高锰酸钾制氧气,则装置A还须稍加改进,改进的方法是__________。用向上排空气法收集氧气,并用带火星的木条检验室否收集满,这是利用了氧气__________、__________的性质。写出一个实验室制氧气的化学方程式__________。
⑶实验室常用加热氯化铵和熟石灰的混合物的方法制氨气,可选用图中的__________装置(填编号)。由于氨气极易溶于水,并且密度比空气 小,所以应该用__________收集。
小,所以应该用__________收集。
20.(9分)某学习小组的同学做实验,向盛有少量氢氧化钠溶液的试管中通入二氧化碳,未看到明显的实验现象。
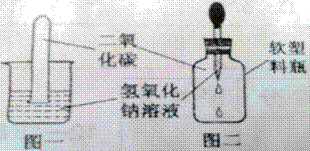
【提出问题】氢氧化钠能否与二氧化碳反应?
【猜想与假设】亮亮同学认为氢氧化钠能与二氧化碳反应;莉莉同学认为氢氧化钠不能与二氧化碳反应。
【设计与实验】亮亮同学设计了两个装置并进行实验。请你和他一起验证他的猜想。
实验步骤 | 实验现象 | 实验结论 |
如图一,将收集满二氧化碳的试管倒置于氢氧化钠溶液中 | ||
如图二,
|
【反思与评价】莉莉同学提出质疑,认为上述现象可能是二氧化碳溶于水的结果。
【设计与实验】请你设计一个实验,证明氢氧化钠确实与二氧化碳反应。
实验步骤 | 实验现象 | 实验结论 |
氢氧化钠与二氧化碳反应 |
【交流与提高】实验证明氢氧化钠还能与二氧化硫反应,化学方程式为:2NaOH+SO2=X+H2O,X的化学式是__________。
宁夏回族自治区2013年初中毕业暨高中阶段招生
化学试题参考答案及评分标准
说明:
1.考生用其它方法做出正确答案的同样得分。
2.化学方程式中化学式(或元素符号)有错误不得分;未配平或未写反应条件扣1分;“↑” 或“↓”漏标两个以上扣1分。
一、选择(选 出下列各题中惟一正确的答案。1—11题每题2分,12—13题每题3分,共28分。不选、多选、错选不得分)
出下列各题中惟一正确的答案。1—11题每题2分,12—13题每题3分,共28分。不选、多选、错选不得分)
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
答案 | D | A | B | D | A | B | C | A | B | C | C | B | D |
二、填空(共14分)
14.
| +2 |
(4分)
2H2O | 2Fe2+ | CaO | NaHCO3 |
15.(4分)
碳氢元素的质量比为3:1(或C:H=3:1)(1分)
CH4+2O2 CO2+2H2O (2分);
CO2+2H2O (2分);
比二氧化碳造成的温室效应更严重(1分)
16.(6分)
⑴3(2分) ⑵Ca(OH)2+K2CO3=CaCO3↓+2KOH(2分) ⑶过滤(2分)
三、应用(共15分)
17.(9分)
⑴
酸的化学性质 | 化学方程式举例 |
Fe2O3+6HCl=2FeCl3+3H2O(2分,其他正确答案均可得分) | |
2NaOH+H2SO4=Na2SO4+2H2O(2分,其他正确答案均可得分) | |
⑤与某些盐反应(1分) |
⑵铁(或Fe)(1分); ②(1分); 可除去暖水瓶内的水垢(1分,其他正确答案均可得分)
⑶氢离子(或H+)(1分)
18.(6分)
⑴解:设黄铜中锌的质量为x

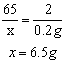
黄铜中铜的质量为:20g-6. 5g=13.5g
5g=13.5g
黄铜中铜的质量分数为: 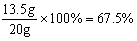
答:(略)
⑵黄铜比纯铜硬度大(1分)
四、实验探究(共18分)
19.(9分)
⑴长颈漏斗(1分); 锥形瓶(1分)
⑵在试管口放团棉花(1分); 密度比空气大(1分); 支持燃烧(1分);
2H2O2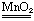 2H2O+O2↑ (2分,其他正确答案均可得分)
2H2O+O2↑ (2分,其他正确答案均可得分)
⑶A(1分); 向下排空气法(1分)
20.(9分)
实验步骤 | 实验现象 | 实验结论 |
试管内页面上升(1分) | ||
如图二,向集满二氧化碳的软塑料瓶中滴加氢氧化钠溶液,振荡(2分) | 塑料瓶变瘪(或向内收缩)(1分) |
实验步骤 | 实验现象 | 实验结论 |
取少量塑料瓶中的液体于试管中,低价稀盐酸(2分) | 有气泡产生(1分) |
(其它正确答案均可得分)
Na2SO3 (2分)


