(单词翻译:单击)
一、选择题(本题共40分,每小题2分,每小题只有一个正确答案)
1.空气中体积分数约为21%的气体是( )
A.氮气 B.氧气 D.稀有气体
2.下列变化中,属于化学变化的是( )
A.胆矾研碎 B.冰雪融化 D.铁生锈
3.下列实验操作中,正确的是( )
A.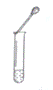 B.
B.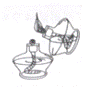
些燃料的燃烧在产生能量的同时会对环境造成影响.下列燃料中,被认为是最清洁燃料的是( )
A.煤 B.石油 D.氢气
5.下列各种物质的用途中,主要利用了其化学性质的是( )
A.活性炭用于净水 B.钨用于制灯泡中的灯丝
D液氮用于医疗上冷冻麻醉.
6.下列有关标志中,与燃烧或爆炸无关的是( )
A. B.
B.
下列有关水的描述中不正确的是( )
A.电解水时在正极产生氧气
B.水是由氢原子和氧原子构成的
软水
D.在沉淀、过滤、蒸馏等净化水的操作中,净化程度最高的是蒸馏
8.下列有关分子、原子、离子的说法正确的是( )
A.分子是保持物质性质的最小粒子 B物质都是由分子构成的
电子构成 D原子得失电子后形成离子
9.“三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体.下图是该反应的微观示意图,其中不同的球体代表不同的原子,下列说法中,不正确的是( )

A.分子在化学变化中可分 B.化学反应前后,原子种类不变
D.参加反应的两种分子的个数比为3:2
10.一些物质的近似pH为:泡菜35性最强的是( )
A.泡菜 B.苹果汁 D.鸡蛋清
11.人体的健康离不开钙元素.下列有关说法不正确的是( )
A.人体中的钙元素主要存在于骨骼和牙齿中
B.钙是人体中含量最高的元素
成年人更多的钙
D.老年人缺钙会造成骨质疏松,容易骨折
12.在奥运比赛中,举重运动员举重前常用白色的“镁粉”搓手,是因为“镁粉”质轻、吸水性好,可作防滑剂.“镁粉”的有效成分是碱式碳酸镁,它不可燃,300℃即分解,其分解的化学方程式是:4 △5
B. D.H2
纸的材料之一.三氧化二铋中铋元素的化合价是( )
A.+6 B.+3 D.-2
14.根据右图提供的信息判断,下列说法正确的是( )

A.钠原子的结构示意图中,
为11
失去电子
D.氯元素为金属元素
15.将80g质量分数为35%的浓盐酸,稀释成10%的稀盐酸,需加水的质量为( )
A.80g B. 100g D.280g
16.实验室要配制50g 10%的氯化钠溶液,其中操作方法不正确的是( )
A.计算所需氯化钠的质量为5g,水的体积为45
g砝码,然后在右盘添加氯化钠至天平平衡,再将氯化钠倒入烧杯中
用玻璃棒搅拌,使氯化钠完全溶解
17.下表中,除去物质所含杂质的方法正确的是( )
物质 | 所含杂质 | 除杂方法 | |
A | 后过滤 | ||
B |
| 氧化铜 | |
C | HCl | 水蒸气 | 将气体通过生石灰 |
D | NaCl溶液 | Na2CO3 | 加适量的氢氧化钙溶液 |
A.A B.B C.C D.D
18.区分下列物质的方法不能达到目的是( )
A.用酚酞试液区分氢氧化钠溶液和碳酸钠溶液
B.用灼烧闻气味的方法来区分天然纤维与合成纤维
C.用磁铁吸引来区分铁丝和铝丝
D.用熟石灰来区分氮肥和钾肥
19.下列有关化学方程式书写不正确的是( )
A.用盐酸除去铁锈:Fe2O3+6HCl═2FeCl3+3H2O
B.镁带在空气中燃烧: Mg+O2 点燃 2MgO2
C.验证铁比铜活泼:Fe+CuSO4═FeSO4+Cu
D.用熟石灰处理工业生产中含硫酸的废水:Ca(OH)2+H2SO4═CaSO 4+2H2O
4+2H2O
20.一定条件下,在一个密闭器内发生某反应,测得反应前后各物质的质量如下表所示,下列说法正确的是( )
物质 | CO2 | O2 | H2O | W |
反应前质量(g) | 6 | 58 | 5 | 23 |
反应后质量(g) | X | 10 | 32 | 0 |
A.该反应属于化合反应
B.W是一种由碳、氢两种元素组成的化合物
C.W是一种由碳、氢、氧三种元素组成的化合物
D.X的值为44
二、填空题(本题共26分,化学方程式每个2分,其他每空1分)
21.用化学符号填空.
(1)2个氮原子 (2)铁离子
(3)锰元素 (4)氢氧化铝中铝显+3价
22.我国南海海底埋藏着丰富的“可燃冰”,“可燃冰”主要为甲烷的水合物,是未来重要的能源甲烷燃烧时,发出明亮的 色火焰,并放出大量的热,反应的化学方程式为。
23.工业的不断发展,逐步提高了人类的生活质量,同时也带来了一系列的环境问题.
(1)化石燃料的大量燃烧,造成大气中的 含量不断上升,从而引起温室效应,同时产生的二氧化硫、二氧化氮等污染物溶于雨水,形成
(2)合成材料的应用和发展,大大方便了人类的生活,但是废弃塑料带来的 也很严重,为了解决这个问题,我们可以采取的措施有 (答一条即可)。
24.如图是A、B、C三种固体物质的溶解度曲线,请根据图示回答.
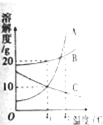
(1)t1时.B的溶解度为 g。
(2)t2℃时,A、B、C三种物质溶解度由大到小的顺序为
(3)要使B从其溶解液中析出最好采取
(4)将t2℃时A、C的饱和溶液降温到t1℃,所得溶液中溶质的质量分 数A
数A
C(填“>”、“=”或“<”)。
25.氢氧化钠有强烈的 性,所以它的俗名叫苛性钠、火碱或烧碱,氢氧化钠固体曝露在空气中时容易吸收水分而溶解,还易与空气中的 发生反应而变质,其反应的化学方程式为  。
。
26.下列物质中,属于混合物的是 (用序号填空,下同),属于单质的是 ,属于化合物的是 ,属于氧化物的是
①生铁 ②冰水混合物 ③纯碱 ④金刚石
27.今年,我国少数地区出现了“甲醛白菜”,就是在白菜上喷洒少量甲醛(CH2O)来保鲜.甲醛有毒,它会破坏 的结构,使其变质.甲醛中碳、氢、氧三种元素的质量比为 ,碳元素的质量分数为 。
三、简答题(本题共10分,每空1分)
28.学好化学可以帮助我们分析和解决生产、生活中的问题.
(1)为了全民的健康,我国推广使用强化铁酱油,这里的“铁”指的是 (填“单质”、“元素”或“原子”)。
(2)校园内铁制车棚易生锈,写出一种防止其生锈的方法: ;同样是金属,为什么金属铝露置在空气中不容易被腐蚀? 在车棚表面喷漆
29.将等质量的锌粉和铁粉,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答:
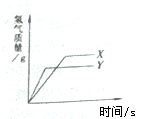
(1)金属X是 ,判断的理由为 。
(2)从图中你还能获得的信息有 (答一条即可)。
30.“化学就在我们身边,它与我们的生活息息相关”.请你用化学知识回答下列问题.
(1)小明奶奶过生日,他和爸爸妈妈送去了鲜花和生日蛋糕.花香满屋,请你从分子的角度解释闻到香味的原因: ,点燃蜡烛许愿后,大家一起将蜡烛吹灭,这种熄灭蜡烛火焰的原理是 。
(2)家庭厨房就是一个化学小世界,“锅碗瓢盆”和“柴米油盐”中包含着许多化学知识。
①下列厨房用品的主要材料中,属于有机合成材料的是 (填代号)

②均衡膳食,有利于人体健康.小恒某天中餐吃了米饭、红烧肉、花生米、水煮鱼,你认为他中餐所吃的食物中缺乏的营养素是 。
四、实验与探究题(本题共16分,化学方程式每个2分,其他每空1分)
31.下面是实验室制取气体及气体性质试验装置图.请回答下列问题:
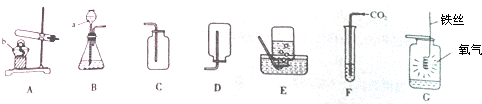
(1)写出图中有标号仪器的名称:a ;b
(2)实验室可用加热氯酸钾和二氧化锰的混合物来制取氧气,其反应的化学方程式为。
(3)如图G,铁丝在氧气中剧烈燃烧, ,生成黑色固体,而瓶底预先放入少量水的目的是 。
(4)实验室制取并收集二氧化碳的装置应选用 (填序号);用图F所示装置来探究二氧化碳能否与水反应,测试管中的水里应加入的试剂是 。
32.某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂。该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体。
【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠 猜想b:碳酸氢钠
小周同学认为猜想b不成立,理由是反应物中没有 元素。
【实验】取少量生成的白色固体于试管中,加入 ,产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊。
稀盐酸(稀HCl)
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式 。
【继续探究】过氧化钠能否与水反应?生成物是什么?
实验步骤 | 实验现象 | 实验结论 |
①取少量过氧化钠粉末于试管中,加入蒸馏水,再用带火星的木条伸入试管中 | 产生气泡 | 过氧化钠能与水反应生成氧气 |
②向上述反应后的试管中滴加酚酞试液 |
溶液变红 | 所得溶液呈碱性,推断过氧化钠与水反应生成 NaOH (填化学式) |
【交流与反思】由于过氧化钠常温下能与二氧化碳和水反应,所以保存过氧化钠一定要
。
五、计算题(本题共8分)
33.如图是某胃药标签上的部分内容,振衡中学化学兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应),共消耗稀盐酸23g,测得反应后烧杯内物质的总质量为25.8g。请计算:

(1)10片药品的质量为 g,反应共生成气体的质量为 g。
(2)药品中碳酸氢钠的质量分数。
(3)反应后所得溶液中溶质的质量分数。(计算结果保留到0.1%)
2012年湖南省衡阳市中考化学试卷参考答案
一、选择题(本题共20小题,每小题2分,共40分)
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
答案 | B | D | C | D | C | A | B | D | D | B |
题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
答案 | B | D | B | B | C | B | B | A | B | C |
二、填空题(本题共26分,化学方程式每个2分,其他每空1分)
21.(1)2N(2)Fe3+(3)Mn(4)Al(OH)3
22. 蓝 CH4+2O2点燃CO2+2H2O
23.(1)二氧化碳 酸雨 (2)白色污染 回收利用废旧塑料
24.(1)20 (2)A>B>C (3)蒸发溶剂 (4)>
25. 腐蚀 二氧化碳或CO2 CO2+2NaOH═Na2CO3+H2O
CO2+2NaOH═Na2CO3+H2O
26.① ④ ②③ ②
27.蛋白质 6:1:8 40%
三、简答题(本题共10分,每空1分)
28.(1)元素 (2)在车棚表面喷漆 铝与氧气反应生成一层致密的氧化膜
29.(1)铁 等质 量的锌粉和铁粉分别放入相同质量分数的足量稀盐酸中,铁产生的氢气比锌多
量的锌粉和铁粉分别放入相同质量分数的足量稀盐酸中,铁产生的氢气比锌多
(2)锌比铁活泼
30.(1)分子在不断运动 降低温度至可燃物着火点以下
(2)①A ②维生素
四、实验与探究题(本题共16分,化学方程式每个2分,其他每空1分)
31.(1)a 长颈漏斗 b酒精灯
(2)2KClO3MnO2△2KCl+3O2↑
(3)火星四射 防止生成的高温熔融物炸裂瓶底
(4)BC 紫色石蕊试液
32. 【猜想】氢(H)
【实验】稀盐酸
【结论】2Na2O2+2CO2=2Na2CO3+O2
【继续探究】①木条复燃 ②溶液变红 NaOH
【交流与反思】密封保存
五、计算题(本题共8分)
33.(1)5 2.2
(2)(3)解:设要生成2.2g二氧 化碳需要参加反应的碳酸氢钠质量为x,
化碳需要参加反应的碳酸氢钠质量为x,
生成氯化钠质量为y,则
NaHCO3+HCl═NaCl+H2O+CO2↑
84 58.5 44
x y 2.2g
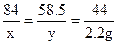 解得x=4.2t y=2.925g
解得x=4.2t y=2.925g
药品中碳酸氢钠的质量分数: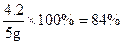
反应后所得溶液质量为:4.2g+23g-2.2g=25g.反应后所得溶液中溶质的质量分数:
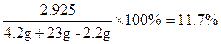
答:(2)药品中碳酸氢钠的质量分数84%;
(3)反应后所得溶液中溶质的质量分数11.7%


