(单词翻译:单击)
一、选择题(本题共15小题,每小题1分,共15分)
33.下列变化中,属于化学变化的是
A.石蜡熔化 B.煤气燃烧 C.汽油挥发 D.玻璃破碎
34.下列气体中,参与植物光合作用的是
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
35.馒头、米饭为人体提供的营养素主要是
A.糖类 B.油脂 C.蛋白质 D.维生素
36.下列化肥中, 属于复合肥料的是
属于复合肥料的是
A. NH4NO3 B. K2CO3C .Ca3(PO4)2 D.(NH4)2HPO4
.Ca3(PO4)2 D.(NH4)2HPO4
37.碘酸钾(KIO3)中碘元素的化合价是
A. +1 B. +3 C. +5 D. +7
38.下列物质中,属于氧化物的是
A.O2 B.P2O5 C.KOH D.CuSO4
39.下列生活用品中 ,由有机合成材料制成的是
,由有机合成材料制成的是
A.陶瓷碗 B.铜火锅 C.塑料瓶D.木桌椅
40.下列物质中,由分子构成的是
A.镁 B.氯化钠 C.金刚石 D.二氧化硫
41.下列物质中,属于石油加工产品的是
A.焦炭 B.柴油 C.煤焦油 D.天然气
42.下列措施中,不利于改善环境的是
A.提倡使用一次性方便筷B.推行“限塑令”
C.推广使用乙醇汽油 D.开发利用太阳能
43.下列做法错误的是
A. 用氮气作焊接金属的保护气B.用酒精溶液作医疗上的消毒剂
C.用洗涤剂清洗餐具上的油污D.用甲醛溶液浸泡海产品
44.下列食物中,酸性最强的是
食物 | 苹果 | 葡萄 | 牛奶 | 豆浆 |
pH | 2.9—3.3 | 3.5— | 6.3—6.6 | 7.4—7.9 |
A.苹果 B.葡萄 C.牛奶 D.豆浆
45.下列做法能够保护水资源的是
A.生活垃圾深埋地下B.用喷灌方式浇灌农田
C.使用含磷洗衣粉D.用化肥代替农家肥
46.下列实验操作正确的是
A.使用前将酒精灯内的酒精装满B.向燃着的酒精灯内 添加酒精
添加酒精
C.用酒精灯的外焰给物质加热D.使用后用嘴吹灭酒精灯
47.下列有关金属的说法中,错误的是
A. 铝具有很好的抗腐蚀性能B.不锈钢可用于制造医疗器械
C.铁是地壳中含量最多的金属元素D.回收利用是保护金属资源的有效途径之一
二、填空题(本题共5小题,每空1分,共24分)
48.化学与生活息息相关。
(1)铁在 ① 的空气中易生锈,防止铁制品锈蚀的一种方法是 ②,用盐酸除铁锈(Fe2O3)的化学方程式为 ③。
(2)医疗上的生理盐水是用① 配制的;人的胃液里含有适量盐酸,可以帮助消化,服用含有②的药物能治疗胃酸过多。
49.右图是某口服液标答的部分内容。

(1)该口服液能为人体提供的一种微量元素是
① ,人体缺乏该元素会引发的病症是② 。
(2)硫酸亚铁的相对分子质量 是① ,硫酸亚铁中铁、硫、氧三种元素的质量比是② 。
是① ,硫酸亚铁中铁、硫、氧三种元素的质量比是② 。
50.2012年6月16日,“神舟九号”载人飞船发射成功。
(1)航天员携带的应急食品采用高强度真空包装。真空包装的食品不易变质的原因是______。
(2)航天员呼吸、排汗产生的水汽被自动收集,冷凝后通过电解制得氧气,反应的化学方程式为① ,制得的氧气可用于②。
(3)航天员的尿液通过“尿液循环器”可转化成高品质的纯净水。要将尿液转化成纯净水,可能用到的净化水的方法有① ,② 。
51.右图是A、B两种固体物质的溶解度曲线。
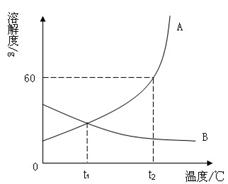
(1)t1℃时,A、B的饱和溶液中溶质的质量分数相等,其原因是________。
(2)t2℃时,60gA溶于100g水,所得溶液(填“是”或“不是”)①饱和溶液,溶液中溶质的质量分数是② 。
(3)分别将A、B的饱和溶液从t2℃降低温度至t1℃,没有晶体析出的是_______的饱和溶液。
52.写出下列反应的化学方程式,并注明反应的基本类型。
(1)碳酸不稳定:、
(2)利用锌和稀硫酸反应制氢气:、
(3)利用红磷燃烧测定空气中氧气的含量:、
三、简答题(本题共5 小题,共25分)
小题,共25分)
53.(3分)用微粒的观点解释下列事实。
(1)相同质量的液态水和气态水所占体积不同。
(2)水中加入少量蔗糖,静置一段时间,最终形成均一、稳定的混合物。
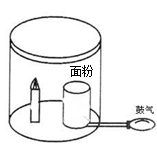
54.(4分)右图是面粉爆炸的实验装置。
(1)点燃蜡烛后,为什么 应立即并快速鼓入大量空气?
应立即并快速鼓入大量空气?
(2)为防止爆炸,面粉加工车间需要保持通风,说明原理。
55.(6分)下图是实验室制取气体常用的两套装置。
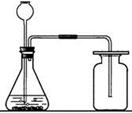
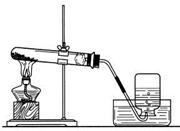
装置A 装置B
(1)选择装置A制 取二氧化碳,反应的化学方程式为①,采用向上排空气法收集二氧化碳的原因是②,验满二氧化碳的方法是③。
取二氧化碳,反应的化学方程式为①,采用向上排空气法收集二氧化碳的原因是②,验满二氧化碳的方法是③。
(2) 选择装置B用高锰酸钾制取氧气,反应的化学方程式为①,收
选择装置B用高锰酸钾制取氧气,反应的化学方程式为①,收 集氧气的方法是②;若实验结束后发现试管破裂,可能的原因之一是③。
集氧气的方法是②;若实验结束后发现试管破裂,可能的原因之一是③。
56.(6分)如右图所示,某河流上游的造纸厂和小型石灰厂,向河中非法排放废液和废渣。通过检测发现:造纸厂排放的废液中含有氢氧化钠和碳酸钠;石灰厂排放的废液显碱性,附近的河水浑浊且水温偏高。
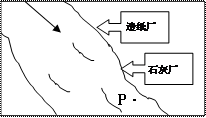
(1)河水温度偏高对水质的直接影响是什 么?为什么?
么?为什么?
(2)在P处取一定量河水,静置后过滤出白色固体;取少量白色固体加入足量稀盐酸,固体全部溶解,并产生使澄清石灰水变浑浊的气体。据此能否确定该白色固体的成分?若能,说明理由;若不能,设计实验确定其成分。
(3)为尽可能减轻河水污染,除了将石灰厂的废渣回收外,还需将两厂的废液集中处理后再排放。简述将两厂废液混合之后还应进行的操作及目的。
57.(6分)工业上可采用多种方法冶炼铜。
(1)在地下利用爆破粉碎孔雀石[Cu2(OH)2CO3],再注入稀硫酸原地浸取,将浸取液抽到地表,加入铁屑制得铜。
冶炼铜的有关化学方程式为①、 ②。
(2)利用一氧化碳还原赤铜矿(Cu2O)冶炼铜。
实验室可用右图所示装置进行实验。
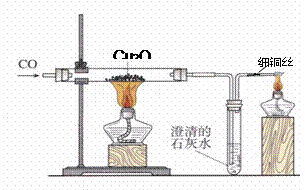
当硬质玻璃管中的反应结束时,应进行的实验操作是①;尾气导管口处的细铜丝,能防止点燃尾气时产生回火引起爆炸,其原理是②。
(3)利用辉铜矿(Cu2S)冶炼铜的原理如下:
Ⅰ.取一定质量的Cu2S在空气中高温焙烧,安全反应后生成一种铜的氧化物和二氧化硫;
Ⅱ.再取上述一半质量的Cu2S,与Ⅰ中生成的铜的氧化物混合均匀,隔绝空气高温煅烧,恰好完全反应,生成铜和二氧化硫。
结合质量守恒定律,判断这种铜的氧化物是什么,写出推理过程。
四、计算题(本题6分)
58.取0.18g炭在一定量氧气中燃烧,全部转化为一氧化碳和二氧化碳的混合气体。将混合气体通入足量石灰水中,充分反应后,得到0.5g碳酸钙。计算:
(1) 混合气体中二氧化碳的质量。
(2) 混合气体中一氧化碳的质量分数。
参考答案
33.B34.D35.A36.D37.C
38.B39.C40.D41.B42.A
43.D44.A45.B46.C47.C
48、⑴潮湿、刷漆等、Fe2O3+6HCl==2FeCl3+3H2O ⑵氯化钠和水、碳酸氢钠等合理答案
49、⑴铁元素、贫血 ⑵ 152、7:4:8
50、⑴隔绝氧气防止食品缓慢氧化(与氧气反应)⑵2H2O 通电 2H2↑+ O2 ↑、供给呼吸⑶过滤、蒸馏、吸附等合理答案
51、⑴t1℃时,A、B溶解度相同 ⑵是、37.5%⑶ B
52、⑴H2CO3=== H2O + CO2↑分解反应 ⑵Zn+H2SO4==ZnSO4+H2↑置换反应
⑶4P + 5O2 点燃 2P2O5化合反应
53、⑴分子间有间隔,质量一定时,液态水和气态水分子个数相同但分子间隔不同,所以体积不同⑵分子间有间隔,蔗糖分子是不断做无规则运动,均匀地分散到水分子中
54、⑴快速鼓入空气,使面粉和空气中氧气充分混合,加快反应速度,短时间放出大量热量,气体快速膨胀,产生爆炸效果⑵ 车间内面粉与氧气混合,如遇到明火,在有限空间内迅速燃烧,短时间放出大量热,有发生爆炸的危险,所以要保持通风,排出面粉颗粒
55、⑴CaCO3+2HCl==CaCl2+H2O+CO2↑、二氧化碳密度大于空气且能溶于水、将燃烧的木条放在集气瓶口看是否熄灭⑵2KMnO4 △ K2MnO4 + MnO2 + O2↑、排水法、先撤走了酒精灯等合理答案
56、⑴河内的鱼虾死亡,温度升高氧气溶解度减小⑵不能,可能有未完全溶解的氢氧化钙,可取少量河水样品加酚酞,看是否变红,若变红则有氢氧化钙存在 ⑶过滤、滤液加适量酸液至PH为中性后排放,防止碱性滤液直接排放(其它合理答案也可)
57、⑴Cu2(OH)2CO3+2H2SO4=2CuSO4+3 H2O+CO2↑、Fe + CuSO4 === FeSO4 + Cu
H2O+CO2↑、Fe + CuSO4 === FeSO4 + Cu
⑵继续通一氧化碳防止新生成的铜被二次氧化铜丝有导热性,吸收部分热量,使温度达不到一氧化碳的着火点
⑶该氧化物为Cu2O,
方法一① Cu2S +O2→ X+ SO2
② 2X+ Cu2S→Cu+SO2
铜有Cu2O和CuO两种氧化物,每分子中氧原子个数为1, ②中因为二氧化硫中S、O个数比1:2,所以X与Cu2S个数比2:1,由题意知①中Cu2S为②中2倍,所以可将①配平如下
2Cu2S +3 O2→2X+2SO2
可知X为 Cu2O
方法二、
假设生成氧化铜
则①Cu2S + 2 O2= 2CuO+ SO2
② 2 CuO + Cu2S= 4Cu+SO2
4Cu+SO2
②中Cu2S用量与①相同,与题意不符
58、⑴0.22g
⑵0.22g×12/44=0.06g(二氧化碳中的碳元素)
0.18g-0.06g=0.12g(一氧化碳中的碳元素)
0.12g÷12/28=0.28g(一氧化碳的质量)
0.28g÷(0.22g+0.28g)=56%

 4.5
4.5
