(单词翻译:单击)
一、选择题(本大题包括15个小题,每小题2分,共30分)每小题只有一个选项符合题意。
1.厨房里的下列操作中,发生了化学变化的是
A.拉面条 B.磨豆浆 C.切黄瓜 D.酿米酒
2.人处于紧张状态时,维生素的消耗会增加,因此考试期间应多补充的食物是
A.馒头 B.蔬菜C.啤酒 D.植物油
3.空气中含有的下列物质属于氧化物的是
A.CO2 B.O2 C.N2D.Ne
4.下列物质中,不属于溶液的是
A.食盐水B.矿泉水 C.蒸馏水 D.冰汽水
5.制作下列仪器时,要用到合成材料的是
A.蒸发皿B.胶头滴管C.燃烧匙 D.集气瓶
6.小明家种的小麦叶色发黄,植株矮小,缺乏氮、磷两种元素,应立即施用的肥料是
A.CO (NH2) 2B.NH4HCO3C. NH4H2PO4
7.用下列矿石冶炼金属时,排放的废气容易引起酸雨的是
A.辉铜矿(主要成分Cu2S)B.赤铁矿(主要成分Fe203)
C.磁铁矿(主要成分Fe304) D.铝土矿(主要成分Al2O3)
8.下列说法中错误的是
A.原子核由质子和电子构成 B.化学变化中原子不能再分
C.分子和原子都在不断运动 D.原子的质量主要集中在原子核上
9.某班同学在对CO 2进行功与过的讨论时,列举的以下事实既可以体现CO2的功,又可以体现CO2的过的是
A.CO2可以使人窒息B.CO2可以作气体肥料
C.CO2可以产生温室效应 D.固体CO2可用于人工降雨
10.亚硝酸钠(NaNO2)是一种工业用盐,虽然有毒但也可以用作防腐剂。NaNO2中氮元素的化合价是
A.+5 B.+3 C.+1D.-3
11.精美的雕花玻璃可以通过氢氟酸(HF)对玻璃的腐蚀作用制成。氢氟酸与玻璃发生反应的化学方程式为:SiO2+4HF= X ↑+2H2O,则X的化学式为
A.F2 B.O2C. SiH4D.SiF4
12.下图是生活中一些常见物质的pH,其中能使无色酚酞溶液变红的是
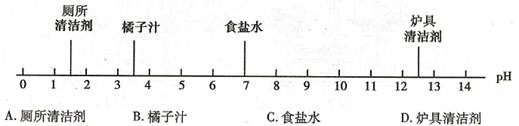
13.物质的性质决定物质的用途,下列描述的物质性质与其对应用途不相符的是
A.浓硫酸有吸水性,可用作干燥剂B.石墨有导电性,可用作电池的电极
C.氧气有助燃性,可用于登山和潜水 D.一氧化碳有还原性,可用于冶炼金属
14.在一定条件下,下列物质中不能与单质碳发生化学反应的是
A.CO B.CO2 C.O2 D.CuO
15.实验室用高锰酸钾制取氧气和用石灰石与稀盐酸制取二氧化碳都不可能用到的装置是
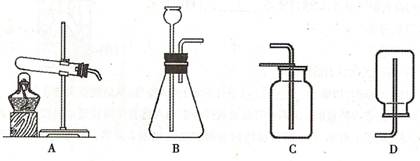
二、填空题(本大题包括6个小题,共22分)
16.(3分)用下列粒子的序号填空。
① 2N②Cl- ③H2
表示分子的是 ,表示离子的是 ,表示金属原子的是 。
17.(4分)水是我们很熟悉的物质,学习化学以后,我们对水有了一些新的认识。
(1)知道了水的微观结构。构成水的粒子可表示为 (填序号)。
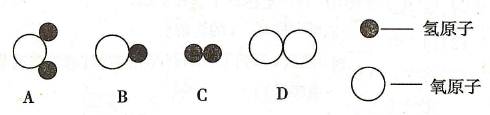
(2)了解了水的宏观组成。水中氢元素的质量分数是。
(3)认识了水的化学性质。写出下列化学反应方程式:
①水中通直流电
②水与生石灰反应
18.(5分)金属材料广泛应用于工业、农业、交通和日常生活等领域。
(1)金属材料包括纯金属以及它们的合金,黄铜(含铜和锌)、生铁都属于 。
(2)将黄铜和生铁分别放人足量的稀盐酸中,浸泡后都有残留固体,其中一种固体一定含,另一种固体一定含。
(3)生铁浸泡在盐酸中发生反应的化学方程式为,该反应的基本类型是。
19.(3分)如下图所示,将白磷和红磷分装于Y形试管的2个支管中,管口系牢小气球,将2个支管同时伸人相同深度的热水中。
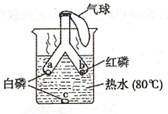
(1)燃烧的是(填“a”、“b”、或“c”)处,该处燃着的磷会很快熄灭,原因可能是 (填序号)。
A.温度降低
B.氧气耗尽白磷
C.试管内产生了二氧化碳气体
(2)管口的小气球可以防止 (填化学式)进人空气,从而使该实验绿色化。
20.(3分)t2℃时,将等质量的a、b两种可溶性固体分别加人盛有相同质量水的烧杯中,充分搅拌后的现象如图I所示,a、b两种物质的溶解度曲线如图2所示。请结合图示回答下列问题:
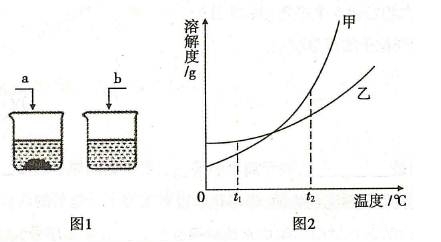
(1)图1中, (填“a”或“b")物质的溶解一定达到了饱和状态。
(2)图2中, (填“甲”或“乙”)表示a的溶解度曲线。
(3)将图1中a溶液的温度从t2℃降低到t1℃,所得溶液与原溶液相比较,通常没有发生变化的是(填序号)。
A.溶液的浓度 B.溶剂的质量C.溶解度
21.(4分)某小组为了验证复分解反应发生的条件,选用了下列部分药品进行实验。
①氢氧化钠溶液②硫酸铜溶液 ③稀盐酸 ④硝酸钾溶液
(1)为了验证有水生成的复分解反应能发生,某同学选择了①和③。你认为除上述四种药品外,还需增加的一种试剂是。
(2)选择 (填序号)两种物质进行实验,能验证有沉淀生成的复分解反应能发生,其化学方程式 。
(3)下列反应中,能验证有气体生成的复分解反应能发生的是 (填序号)。
A.锌与稀硫酸反应 B.天然气燃烧
C.石灰石与稀盐酸反应 D.过氧化氢分解
三、实验题(本大题包括2个小题,共12分)
22.(6分)以下是氯化钠溶液的配制和粗盐中难溶性杂质的去除(需要计算粗盐的产率)实验活动中的部分操作。
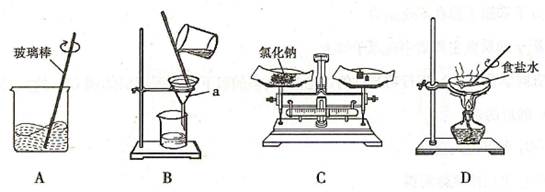
(1)仪器a的名称是 。
(2)配制6%的氯化钠溶液和粗盐中难溶性杂质的去除都要用到的实验操作是 (填序号)。
(3)A中玻璃棒搅拌的作用是使氯化钠 。如果B中的滤液仍然浑浊,就应该。D操作中,当观察到蒸发皿中出现 时,停止加热。
23.(6分)某班同学按下图所示的实验探究质量守恒定律。
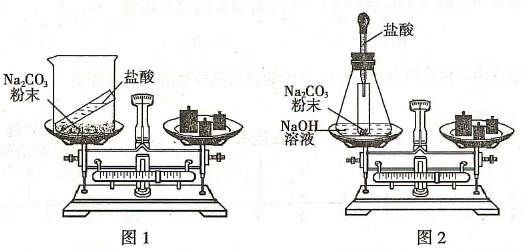
(1)同学们先按图1的方式实验,将盐酸加到碳酸钠粉末中发生反应的化学方程式为 。该实验中,大家进行了两次称量,有四个小组得到下列数据,其中有问题的两组数据是 (填序号)。
A | B | C | D | |
盐酸加入Na2 CO3粉末前称量/g | 85.3 | 82.8 | 84.8 | 86.5 |
盐酸加入Na2 CO3粉末后称量/g | 85.3 | 80.6 | 83.2 | 87.8 |
(2)同学们又按照图2的方式实验,当天平平衡后,挤压胶头滴管逐滴滴人盐酸,最终天平的状态是 (填序号)。
A..左盘高B.右盘高C.保持平衡
该实验中通过化学反应新生成了的物质有(填序号)。
A.HC1 B.CO2 C.Na2CO3D.NaOH
四、计算题(本大题包括1个小题,共6分)
24.葡萄糖(C6H12O6)是人体重要的供能物质,每克葡萄糖完全代谢释放的能量为16 kJ(表示为16 kJ/g)。葡萄糖在体内代谢的化学方程式为:C6H12O6 +6O2 酶6CO2+6H2O。某病人需要输入5%的葡萄糖注射液500 mL(密度近似为1g/cm3)。计算:
(1)配制上述注射液所需20%的葡萄糖溶液的质量、蒸馏水的质量。
(2)若上述注射液中的葡萄糖完全代谢,理论上消耗氧气的质量是多少?释放出的能量是多少?
重庆市2013年中考化学参考答案及评分意见
一、选择题(每小题2分,共30分)
1.D 2 .B3.A 4.C 5.B 6.C 7.A 8.A 9.C 10.B 11.D12.D13.C14.A15.D
二、 填空题(共22分)
16.(3分)
③(1分) ②(1分) ④(1分)
17.(4分)
⑴ A(1分)
⑵ 11.1%(1分)
⑶ ①2 H2O 通电 2 H2↑+ O2↑(1分)②CaO+H2O =Ca(OH)2(1分)
18.(5分)
⑴ 合金(1分)
⑵ 铜(或Cu)碳(或C)(顺序可颠倒)(各1分)
⑶ Fe + 2 HCl = FeCl2 + H2↑(1分) 置换反应(1分)
19.(3分)
⑴ a(1分)B(1分)
⑵ P2O5(1分)
20.(3分)
⑴ a(1分) ⑵ 乙(1分)⑶ B(1分)
21.(4分)
⑴酚酞溶液(或指示剂、或石蕊溶液等)(1分)
⑵ ①②(1分)CuSO4+2NaOH== Cu(OH)2↓+ Na2SO4(1分) C(1分)
三、实验题(共12分)
22.(6分)
⑴漏斗(1分)
⑵AC(1分)
⑶加速溶解(1分) 再过滤一次(1分) 较多固体(1分)
23.(6分)
⑴Na2CO3+2HCl==2NaCl+H2O+CO2↑(1分) AD(1分)
⑵ C(1分)BC(2分)
四、计算题(共6分)



