(单词翻译:单击)
一、选择题(本题包括10小题,每小题2分,共20分.在每小题给出的四个选项中只有一个选项是符合题目要求的
1.(2012•呼和浩特)下列物质的用途与其化学性质相关的是( )
A. 用铝作导线 B. 用汽油去除衣物上的油污
C. 用天然气作燃料煮饭 D. 用氦气填充探空气球
2.(2012•呼和浩特)下列说法正确的是( )
A. 煤气泄漏立即打开抽油烟机排气
B. 用焚烧法可以处理塑料垃圾
C. 用过滤的方法能使硬水软化
D. 羊毛和合成纤维都属于高分子化合物
3.(2012•呼和浩特)目前常用的消毒剂有氯气(Cl2)、二氧化氯(ClO2)、漂白粉【主要含Ca(ClO)2】等,这三种物质都含有( )
A. 氯元素  B. 氯分子 C. 氯离子 D. 氯单质
B. 氯分子 C. 氯离子 D. 氯单质
4.如图所示装置也可用来测定空气中氧气的含量.对该实验认识不正确的是( )
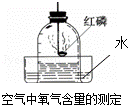
A. 红磷的量不足会影响实验结论
B. 装置不漏气是实验成功的重要因素之一
C. 将红磷改为碳也能得到正确的实验结论
D. 钟罩内气体压强的减小会导致水面的上升
5.(2012•呼和浩特)下列实验方法错误的是( )
A. 用适量的水区分NH4NO3固体和NaOH固体
B. 用紫色石蕊溶液鉴别二氧化碳气体和一氧化碳气体
C. 稀释浓硫酸时,应将浓硫酸沿容器壁慢慢注入水中,并不断搅拌
D. 把燃着的木条伸入某无色气体的集气瓶中,火焰熄灭,该气体一定是二氧化碳气体
6.(2012•呼和浩特)下列有关生产、环保、资源问题叙述错误的是( )
A. 长期使用硫酸铵会使土壤呈酸性,应将硫酸铵与熟石灰混合使用
B. “温室效应”主要是由二氧化碳等气体引起的
C. pH<5.6的酸性降水称为酸雨,它的形成与大气中SO2等酸性污染物增多有关
D. 煤和石油是不可再生资源,必须综合利用以提高利用率
7 .物质的结构决定物质的性质,下列关于物质结构与性质的说法不正确的是( )
.物质的结构决定物质的性质,下列关于物质结构与性质的说法不正确的是( )
A. 生铁和钢的性能不同,主要是由于含碳量的不同
B. CO和CO2的性质不同,是由于构成它们的分子不同
C. 金刚石和石墨的物理性质不同,由于构成它们的碳原子不同
D. 金属钠和镁的性质不同,是由于钠和镁的原子结构不同
8.(2012•呼和浩特)以下叙述正确的是( )
A. 由不同元素组成的物质一定是化合物
B. 含有氧元素的化合物是氧化物
C. 燃烧都是剧烈的发光发热的化合反应
D. 分子是构成物质的一种微粒
9.(2012•呼和浩特)三甲基一氯硅【(CH3)3SiCl】是一种生产有机硅化合物的原料,遇明火会引起爆炸,在空气中燃烧生成一氧化碳、二氧化碳、二氧化硅和氯化氢,三甲基一氯硅与水接触可产生雾状盐酸.则下列说法错误的是( )
A. 保存三甲基一氯硅时应密封防水
B. 三甲基一氯硅溶于水,所得溶液pH一定小于7
C. 扑灭三甲基一氯硅引发着火,应使用二氧化碳或干粉灭火剂
D. 三甲基一氯硅由碳、氢、硅、氯四种原子构成
10.(2012•呼和浩特)下列各组变化中,每一转化在一定条件下均能一步实现的是( )
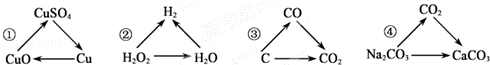
A. ①③ B. ①③④ C. ②③④ D. ①②③④
二、填空题(本题包括5个小题,共15分)
11.(2012•呼和浩特)化学就在我们身边,它能改善我们的生活.请从“小苏打、氮气、烧碱、生石灰”中选择合适的物质用化学式填空:
(1)食品包装袋内的干燥剂 _________ .
(2)烙制糕点所用发酵粉的主要成分之一是 _________ .
答案为:(1)CaO;(2)NaHCO3;
12.(2012•呼和浩特)下列两组物质,请将满足题意的物质的化学式填在答题纸上
(1)石灰石、臭氧、石油、稀盐酸中属于纯净物的是 _________ .
(2)NO、KNO3、N2O4、NaNO2、NH3中氮元素化合价最高的物质是 _________ .
答案为:(1)O3;(2)KNO3.
13.(2012•呼和浩特)氢化钙(CaH2)固体可用于登山队员的能源提供剂,与氢气做能源相比它的优点是 _________ ;它和水反应生成氢氧化钙和氢气,则该反应的化学方程式为 _________ .
答案为:携带方便;CaH2+2H2O═Ca(OH)2+2H2↑.
14.(2012•呼和浩特)溶液的应用非常广泛.
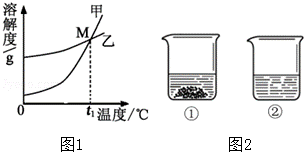
K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下:
温度/℃ | 20 | 30 | 50 | 60 | 80 | |
溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
(2)曲线上M点的含义是 _________ .
(3)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.
下列有关说法中,正确的是 _________ (填字母).
A、烧杯②中溶液是不饱和溶 液
液
B、升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
C、若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小
D、将得到的烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能不变.
 15.(2012•呼和浩特)海洋中有丰富的资源,如图所示利用海水可获得许多化工产品.
15.(2012•呼和浩特)海洋中有丰富的资源,如图所示利用海水可获得许多化工产品.
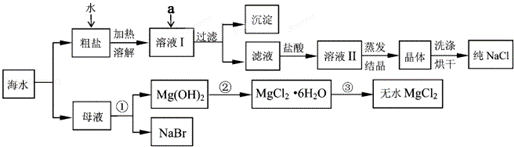
(1)粗盐中除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质.欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液中选出a所代表的试剂,按滴加顺序依次为: _________ 、过量的BaCl2溶液、 _________ .加入BaCl2溶液发生反应的化学方程式为 _________ .
(2)在滤液中加盐酸的作用是 _________ .
(3)第③步发生的基本反应类型是 _________  反应.
反应.
15.(1)过量的NaOH溶液;过量碳酸钠溶液;BaCl2+Na2SO4═BaSO4↓+2NaCl;
(2)除去溶液中的NaOH、Na2CO3;(3)分解
三、实验题(本题包括2个小题.共10分)
16.(2012•呼和浩特)某研究小组的同学为探究铝、铁、铜、锌的金属活动顺序,设计了如图所示的四个实验(其中金属均已用砂纸打磨,且形状、大小相同;所用稀盐酸的溶质质量分数、用量也相同).
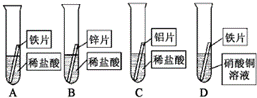
(1)通过观察,甲同学很快判断出锌、铁、铝活动性强弱.据你分析,甲同学依据的实验现象是 _________ .过一会儿,他又发现D中铁片表面有红色固体附着,这说明 _________ .
(2)实验时选用Zn而不用AI、Fe制取氢气的原因是 _________ .
A试管中的实验现象为 _________ .
(3)铝比铁的活动性强,易氧化,但是为什么铝制品耐用而铁制品却容易锈蚀 _________ .
答案:(1)在A、B、C中生成气体的速率不同;铁的金属活动性强于铜;(2)锌和酸反应生成氢气速度适中;有气泡产生,铁片逐渐溶解,溶液有无色变为浅绿色;
(3)因为铝在常温下氧化生成致密的氧化物保护膜;
17.(2012•呼和浩特)下列各图是进行O2、CO2的实验室制取和有关性质的实验装置.
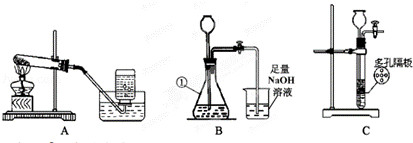
(1)写出标号①的仪器名称: _________ .
(2)用氯化钾固体制取O2,应选用上图中的 _________ 装置(填字母);反应的化学方程式为 _________ .
(3)用稀盐酸和大理石在B装置中反应制取CO2并检验其有关性质,观察到烧杯中导管口有气泡冒出,但无其它明显现象.若证明CO2与NaOH溶液发生了化学反应,以下方案不合理的是 _________ (填序号).
①取少量烧杯中液体滴加无色酚酞
②取少量烧杯中液体滴加足量稀盐酸
③取少量烧杯中液体滴加氯化钙溶液
(4)用C装置代替B中的气体发生装置制备CO2,优点是 _________ .
答案:(1)锥形瓶(2)A;2KClO3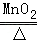 2KCl+3O2↑.(3)①(4)可随时控制反应的发生和停止.
2KCl+3O2↑.(3)①(4)可随时控制反应的发生和停止.
四、计算题(本题仅有一个小题,共5分)
18.(2012•呼和浩特)请根据如图所示实验过程和数据计算:
(1)反应中生成氢气的质量
(2)反应后溶液中H2SO4的质量为 _________ g.

答案:解:设生成氢气的质量为x,参加反应的H2SO4的质量为y
Zn+H2SO4=ZnSO4+H2↑
65 98 2
13g y x
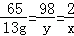
解得y=19.6g x=0.4g
设原硫酸溶液的质量为z
溶液质量的计算方法是z+13g﹣0.4g=162.6g,解得z=150g,
剩余H2SO4的质量=162.6g×20%﹣19.6g=10.4g
答:反应中生成氢气的质量0.4g,反应后溶液中H2SO4的质量为10.4g.


