(单词翻译:单击)
一、选择题(本大题共8个小题,每小题3分,共24分,每题只有一个选项符合题目要求)
7.掌握物质的分类是学习化学的基础,下列物质中属于盐的是( A )
A.NaCl B.KOH C.MgO D.Cu
8.下列说法中不正确的是( D )
A.硬水中加入肥皂水容易起浮渣 B.用洗洁精洗去餐具上的油污属于乳化
C.用酒精洗去试管中的碘属于溶解 D.空气中氮气的质量分数为78%
9.右图是元素周期表中某元素的相关信息,从图中不能直接获得的信息是( D )
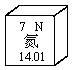
A.该元素属于非金属元素
B.该元素的原子序数为7
C.该元素的相对原子质量是14.1
D.氮气的化学式为N2
10.下列物质的俗称或名称与其化学式不相符合的是( C )
A.干冰CO2 B.熟石灰Ca(OH)2 C.小苏打Na2CO3 D.氦气He
11.保护环境人人有责,下列措施与保护环境无关的是( C )
A.提倡乘坐公共交通、骑自行车或步行的方式出行
B.推广使用太阳能、风能等清洁能源
C.减少户外运动时间,避免呼吸道疾病
D.废旧电池回收集中处理
12.下列说法正确的是( D )
A.钾肥不但能促进农作物枝叶茂盛,叶色浓绿,还能提高产量
B.CO2的排放是导致酸雨的主要原因
C.合金、塑料、橡胶等都是重要的有机合成材料
D.防止金属腐蚀是保护金属资源的有效途径
13.下列实验方案或措施合理的是( B )
A.除去CaO中混有的CaCO3,先加足量的水,然后过滤
B.除去MnO2粉末中混有的KCl,加足量的水溶解、过滤、洗涤、干燥
C.用无色酚酞溶液检验氢氧化钠溶液是否变质
D.用碘化钾溶液检验食品中是否含有淀粉
14.某有机物R和氧气置于完全封闭的容器中引燃,充分反应后,生成二氧化碳和水。实验测得反应前后物质质量如下表:
R | O2 | CO2 | H2O | |
反应前质量(g) | 51 | 96 | 0 | 0 |
反应后质量(g) | x | 0 | 88 | 54 |
下列说法中不正确的是( B )
A.x的值为5
B.R物质中只含有碳、氢元素
C.R物质中碳氢元素的质量比为4∶1
D.反应生成的二氧化碳和水的分子个数比为2∶3
五、(本大题共4个小题,每空1分,共17分)
40.下图是自然界中碳、氧循环的简图,请回答:
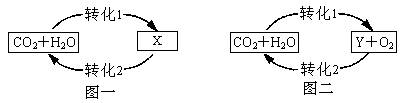
(1)图一中,转化1表示水吸收二氧化碳的过程,发生反应的化学反应方程式为 CO2+H2O=H2CO3
(2)图二中,转化1是自然界中碳、氧循环的重要反应之一—绿色植物光合作用的过程,反应的化学方程式为: (6CO2+6H2O叶绿体光C6H12O6+6O2)
(3)上述反应中两个反应的反应物相同,但得到的产物却完全不同,原因是 反应的条件不同 。
41.某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示,请回答有关问题:
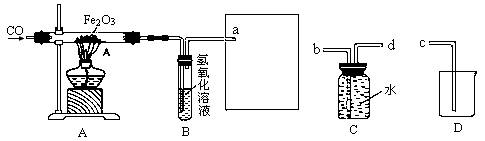
(1)实验进行一段时间之后,A玻璃管内观察到的现象是 红色粉末变为黑色
(2)B装置中氢氧化钠溶液的作用是 吸收CO2 。
(3)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→ d→b→c
(4)除CO外,还有氢气等物质可以还原Fe2O3,某同学设计了用金属锌粒与稀硫酸反应制取氢气的实验装置,如右图所示:
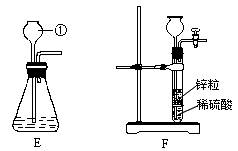
①制取氢气的反应方程式为Zn+H2SO4=ZnSO4+H2↑
②用E和F装置制取二氧化碳,F装置与E装置比较,优点是能使反应随时发生随时停止
42.根据下列数型图像回答:
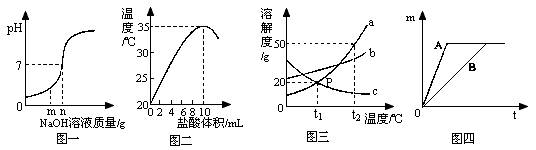
(1)图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线。向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为 H+、Na+、Cl- (填离子符号)
(2)图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系
①由图可知中和反应是放热反应,你的依据为 反应过程中温度不断升高,完全反应时放出的热量最多
②甲同学用氢氧化钠固体与稀盐酸反应也能得到相同结论,乙同学认为不严密,因为 氢氧化钠固体溶于水时也要放出热量
(3)图三是a、d、c三种物质的溶解度曲线。a与c的溶解度相交于P点,据图回答:
①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用 降低温度 的方法达到饱和状态
②将t2℃时,150g a物质的饱和溶液降温到t1℃时。可以析出 30 g a物质。
(4)右图托盘天平两边是等质量的铁和镁分别跟等质量等浓度的稀硫酸反应,反应时间t与生成氢气质量m的变化关系如图四。
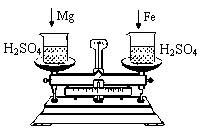
试回答:从开始反应到不再产生气体为止,天平指针偏转情况是 先偏向右边,最后回到分度盘中央
43.核电荷数为1~18的元素原子结构示意图等信息如下,
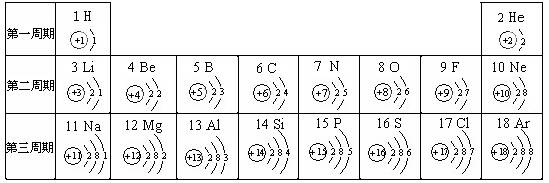
回答下列问题:
(1)氧元素与硫元素化学性质相似,主要是因为 最外层电子数相同
(2)写出由8号,13号元素组成的化合物的化学式 Al2O3
六、(本大题共2个小题,共10分,其中44题2分,45题8分)
44.回答下列问题:

(1)阅读右图包装说明,这袋化肥中碳酸氢铵的质量为 47.4 g
(2)欲将50kg10%的碳酸氢铵溶液稀释成1%的溶液,用于农作物的催肥,需加 450 g水。
45.某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图
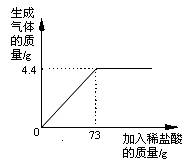
(1)纯碱恰好完全反应时,生成CO2的质量为 4.4 g
(2)计算该样品中含杂质的质量分数是多少?(计算结果保留一位小数,下同)
(3)计算当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是多少?
解:社样品中含Na2CO3的质量为x,反应生成NaCl的质量为y
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 117 44
x y 4.4
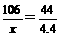
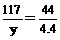
∴x=10.6(g) y=11.7(g)
(2)样品中含杂质的质量分数为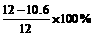 =11.7%
=11.7%
(3)当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数为
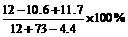 =16.3%
=16.3%
答:(略)
七、(本大题3个小题,每空1分,共14分)
46.有一包白色粉末可能由NaCl、NaNO3、MgCl2、CuSO4、中的一种或多种物质组成。小明为了探究其成分,设计并完成了如下图所示的实验。
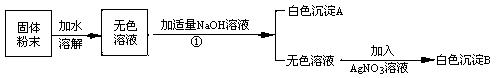
根据以上实验,回答:
(1)操作①是 过滤
(2)原固体粉末中一定没有的成分是 CuSO4
(3)生成沉淀A的化学方程式是 MgCl2+2NaOH=Mg(OH)2↓+2NaCl
(4)根据上述实验 不能 (填‘能’或‘不能’)确定原固体粉末中含有NaCl、NaNO3。
47.(1)铝合金应用广泛,抗腐蚀性强,是因为 铝表面有致密的氧化铝保护膜
(2)将铁粉加入CuSO4溶液中,充分反应后过滤,向所得物体加入稀盐酸,产生气泡,则滤纸上的物质是 Cu、Fe ,溶液中的溶质是 FeSO4
48.同学们利用“硫酸、硝酸铵、氢氧化钠、碳酸钾”四种物质的溶液进行探究学习,完成下列各问:
【实验探究】
(1)A、B、C、D四组同学分别进行了下列实验
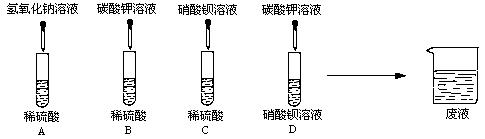
写出下列的两个化学方程式:
①A中的反应 H2SO4+2NaOH=Na2SO4+2H2O
②D中的反应 K2CO3+Ba(NO3)2=BaCO3↓+2KNO3
【挖掘实质】
右图是A组反应的微观过程示意图该化学反应的实质可以表示为H++OH-=H2O
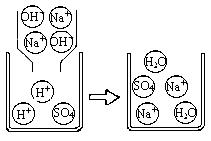
【实践运用】
完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色。
(1)①溶液中的白色沉淀一定是 BaSO4 ,理由是 BaSO4与酸不反应,而BaCO3要与酸反应
(2)废液中一定不含有的离子是 OH- CO32-
(3)为了验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证
溶液中可能含有的离子 | 实验步骤 | 实验现象 | 实验结论 |
可能含有SO42- | ②取滤液滴加Ba(NO3)2 溶液 | 现象明显 | 含有该离子 |


