(单词翻译:单击)
第1卷(必做,共88分)
一、选择题(本题包括l5小题,每小题只有一个选项符合题意)
1.从细胞膜上提取了某种成分.用非酶法处理后.加人双缩脲试剂出现紫色;若加入斐林或班氏试剂并加热,出现砖红色。该成分是
A糖脂B磷脂C糖蛋白D脂蛋白
2.已知分泌蛋白的新生肽链上有段可以引导其进入内质网的特殊序列(图中P肽段)。若P肽段功能缺失,则该蛋白
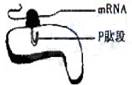
A.无法继续合成
B.可以进入高尔基体
C.可以被加工成熟
D.无法被分泌到细胞外
3. 2008年1月12日我国科考队员登上了南极“冰盖之巅”。他们生理上出现的适应性变化是
①体温下降②机体耗氧量降低
③皮肤血管收缩④体温调节中枢兴奋性增强
⑤甲状腺激素分泌量增加
A①③④B①④⑤C②③⑤D.③④⑤
4通过特定方法,科学家将小鼠和人已分化的体细胞成功地转变成了类胚胎干细胞。有关分化的体细胞和类胚胎于细胞的描述,正确的是
A.粪胚胎干细胞能够分化成多种细胞B分化的体细胞丢失了某些基因
C二者功能有差异,但形态没有差异D二者基因组相同,且表达的基因相同
5下列与生物进化相关的描述,正确的是
A进化总是由突变引起的B进化时基因频率总是变化的
C变异个体总是适应环境的D进化改变的是个体而不是群体
6分裂期细胞的细胞质中含有一种促进染色质凝集为染色体的物质。将某种动物的分裂期细胞与G1期(DNA复制前期)细胞融合后,可能出现的情况是
A来自G1期细胞的染色质开始复制B融合细胞ONA吉量是G1期细胞的2倍
C来自G1期细胞的染色质开始凝集D融合后两细胞仍按各自的细胞周期运转
7 右图所示为叶绿体中色索蟹白等成分在膜上的分布。在图示结构上
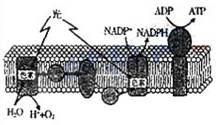
A生物膜为叶绿体内膜
B可完成光合作用的全过程
C发生的能量转换是:光能→电能→化学能
D产生的ATP可用于植物体的各项生理活动
8拟南芥P基因的突变体表现为花发育异常。用生长素极性运输抑制剂处理正常拟南芥,也会造成相似的花异常。下列推测错误的是
A生长素与花的发育有关
B生长素极性运输与花的发育有关
C P基因可能与生长素极性运输有关
D生长索极性运输抑制剂诱发了P基因突变
9下列叙述合理的是
A金属材料都是导体,非金属材料都是绝缘体
B棉、麻、丝、毛及合成纤维完全燃烧都只生成CO,和H2O
C水电站把机械能转化成电能,而核电站把化学能转化成电能
D我国规定自2008年6月l日起,商家不得无偿提供塑料袋,目的是减少“白色污染”
10下列由事实得出的结论错误的是
A维勒用无机物合成了尿素,突破了无机物与有机物的界限
B门捷列夫在前人工作的基础上发现了元素周期律,表明科学研究既要继承又要创新
C C60是英国和美国化学家共同发现的,体现了国际科技合作的重要性
D科恩和渡普尔因理论化学方面的贡献获诺贝尔化学奖,意味着化学已成为以理论研究主的学科
11下列说法正确的是
A SiH4比CH4稳定
B 02-半径比F-的小
C Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强
D P和As属于第ⅤA族元素.H3PO4酸性比H3AsO4的弱
12下列叙述正确的是
A汽油、柴油和植物油都是碳氢化合物
B乙醇可以被氧化为乙酸,二者都能发生酯化反应
C甲烷、乙烯和苯在工业上都可通过石油分馏得到
D含5个碳原子的有机物,每个分子中最多可形成4个C—C单键
13 NA代表阿伏加德罗常数,下列叙述错误的是
A生10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2s04的质量分数为9.8%
B在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子
C标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D一定温度下,l L 0.50 mol·L-1NH4Cl溶液与2 L0.25 mol·L°NN4Cl溶液含NH4+物质的量不同
14高温下,某反应达平衡,平街常数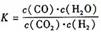 恒容时,温度升高.H2浓度减小。下列说法正确的是
恒容时,温度升高.H2浓度减小。下列说法正确的是
A该反应的焓变为正值
B恒温恒容下,增大压强,H2浓度一定减小
C升高温度,逆反应速率减小
D该反应化学方程式为
15某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
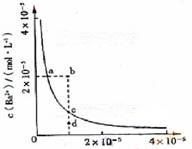
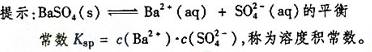
A加入Na2SO4可以使溶液由a点变到b点
B通过蒸发可以使溶液由d点变到c点
C d点无BaSO4沉淀生成
D a点对应的KaP大于c点对应的KaP
二、选择题(本题包括7小题,每小题给出的四个选项中,有的只有一个选项正确.有的有多个选项正确,全部选对的得4分,选对但不全的得2分,有选错的得0分)
16用轻弹簧竖直悬挂质量为m的物体,静止时弹簧伸长量为L0现用该弹簧沿斜面方向拉住质量为2m的物体,系统静止时弹簧伸长量也为L0斜面倾角为300,如图所示。则物体所受 摩擦力
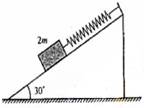
A等于零
B大小为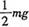 ,方向沿斜面向下
,方向沿斜面向下
C大小为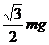 ,方向沿斜面向上
,方向沿斜面向上
D大小为mg,方向沿斜面向上
17质量为1500kg的汽车在平直的公路上运动,v-t图象如图所示。由此可求
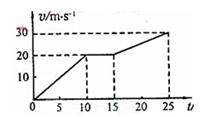
A前25s内汽车的平均速度
B前l0s内汽车的加速度
C前l0s内汽车所受的阻力
D15~25s内台外力对汽车所做的功
18据报道,我国数据中继卫星“天链一号Ol星”于2008年4月25日在西昌卫星发射中心发射升空,经过4次变轨控制后,于5月1日成功定点在东经770赤道上空的同步轨道。关于成功定点后的“天链一号01星”,下列说法正确的是
A运行速度大于7.9 km/s
B.离地面高度一定,相对地面静止
C绕地球运行的角速度比月球绕地球运行的角速度大
D向心加速度与静止在赤道上物体的向心加速度大小相等
19直升机悬停在空中向地面投放装有救灾物资的箱子,如图所示。设投放初速度为零.箱子所受的空气阻力与箱子下落速度的平方成正比,且运动过程中箱子始终保持图示姿态。在箱子下落过程中.下列说法正确的是
A箱内物体对箱子底部始终没有压力
B箱子刚从飞机上投下时,箱内物体受到的支持力最大
C箱子接近地面时,箱内物体受到的支持力比刚投下时大
D若下落距离足够长,箱内物体有可能不受底部支持力而“飘起来”
20图1、图2分别表示两种电压的波形,其中图1所示电压按正弦规律变化。下列说法正确的是
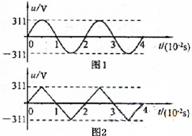
A图l表示交流电,图2表示直流电
B两种电压的有效值相等
C图1所示电压的瞬时值表达式为u=311 sinl00πt
D图1所示电压经匝数比为10:l的变压器变压后,频率变为原来的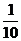
21如图所示,在y轴上关于0点对称的A、B两点有等量同种点电荷+Q,在x轴上C点有点电荷-Q且CO=OD,∠ADO=600。下列判断正确的是
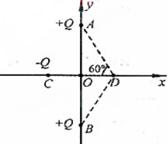
A O点电场强度为零
B D点电场强度为零
C若将点电荷+q从O移向C,电势能增大
D若将点电荷-q从O移向C,电势能增大
22两根足够长的光滑导轨竖直放置,间距为L,底端接阻值为R的电阻。将质量为m的金属棒悬挂在一个固定的轻弹簧下端,金属棒和导轨接触良好.导轨所在平面与磁感应强度为B的匀强磁场垂直,如图所示。除电阻R外其余电阻不计。现将金属棒从弹簧原长位置由静止释放,则
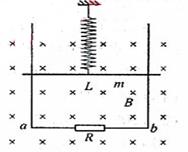
A 释放瞬间金属棒的加速度等于重力加速度g
B金属棒向下运动时,流过电阻R的电流方向为a→b
C金属棒的速度为v时,所受的安培力大小为F=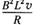
D电阻R上产生的总热量等于金属棒重力势能的减少
第Ⅱ卷(必做120分+选做32分,共152分)
【必做部分】
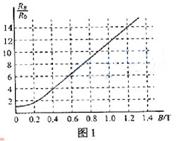
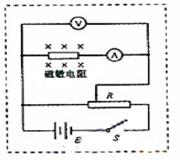
23(12分)2007年诺贝尔物理学奖授予了两位发现“巨磁电阻”救应的物理学家。材料的电阻随磁场的增加而增大的现象称为磁阻效应,利用这种效应可以测量磁感应强度。若图l为某磁敏电阻在室温下的电阻一磁感应强度特性曲线,其中RB,R0分别表示有、无磁场时磁敏电阻的阻值。为了测量磁感应强度B,需先测量磁敏电阻处于磁场中的电阻值RB。请按要求完成下列实验。
(1)设计一个可以测量磁场中该磁敏电阻阻值的电路,在图2的虚线框内画出实验电路原理图(磁敏电阻及所处磁场已给出,待测磁场磁感应强度大小约为0.6~1.0T,不考虑磁场对电路其它部分的影响)。要求误差较小。
提供的器材如下:
A磁敏电阻,无磁场时阻值Ro=150Ω
B滑动变阻器R,全电阻约20Ω
C电流表.量程2.5mA,内阻约30Ω
D电压表,量程3V,内阻约3kΩ
E直流电源E,电动势3V,内阻不计
F开关S,导线若干
(2)正确接线后,将磁敏电阻置入待测磁场中,测量数据如下表
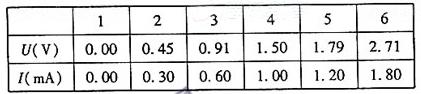
根据上表可求出磁敏电阻的测量值RB=________Ω,
结合图1可知待测磁场的磁感应强度B=_________T。
(3)试结合图1简要回答,磁感应强度B在0~0.2T和0.4~1.0T范围内磁敏电阻阻直的变化规律有何不同?
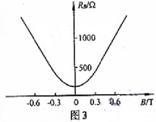
(4)某同学查阅相关资料时看到了图3所示的磁敏电阻在一定温度下的电阻一磁感应强度特性曲线(关于纵轴对称),由图线可以得到什么结论?
(1)如右图所示
(2)1500 0.90
(3)在0~0 2T范围内,磁敏电阻的阻值随磁感应强度非线性变化(或不均匀变化);在0.4~1.0T范围内,磁敏电阻的阻值随磁感应强度线性变化(或均匀变化)
(4)磁场反向.磁敏电阻的阻值不变。
24(15分)某兴趣小组设计了如图所示的玩具轨道,其中“2008”四个等高数字用内壁光滑的薄壁细圆管弯成,固定在竖直平面内(所有数字均由圆或半圆组成,圆半径比细管的内径大得多),底端与水平地面相切。弹射装置将一个小物体(可视为质点)以Va=5m/s的水平初速度由a点弹出,从b点进入轨道,依次经过“8002”后从p点水平抛出。小物体与地面ab段间的动摩擦因数μ=0.3,不计其它机械能损失。已知ab段长L=l.5m,数字“0”的半径R=0.2m,小物体质量m=0.0lkg,g=10m/s2。求:

(1)小物体从p点抛出后的水平射程。
(2)小物体经过数字“0”的最高点时管道对小物体作用力的大小和方向。
解:(1)设小物体运动到p点时的速度大小为v,对小物体由a运动到p过程应用动能定理得 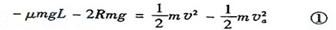 小物体自P点做平抛运动,设运动时间为t.水平射程为s,则
小物体自P点做平抛运动,设运动时间为t.水平射程为s,则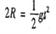 ②
②
s=vt③
联立①②③式,代入数据解得s=0.8m④
(2)设在数字“0”的最高点时管道对小物体的作用力大小为F取竖直向下为正方向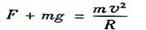 ⑤
⑤
联立①⑤式,代入数据解得
F=0.3N⑥
方向竖直向下
25(I 8分)两块足够大的平行金属极板水平放置,极板间加有空间分布均匀、大小随时间周期性变化的电场和磁场,变化规律分别如图1、图2所示(规定垂直纸面向里为磁感应强度的正方向)。在t=0。时刻由负极板释放一个初速度为零的带负电的粒子(不计重力)。若电场强度E0、磁感应强度B0、粒子的比荷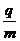 均已知,且
均已知,且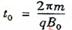 ,两板间距h=
,两板间距h=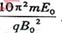 。
。
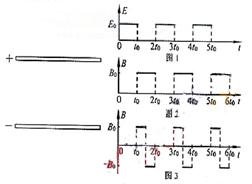
(1)求粒子在0~to时间内的位移大小与极板间距h的比值。
(2)求粒子在极板间做圆周运动的最大半径(用h表示)。
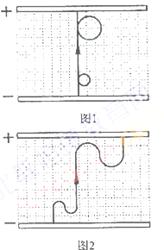
(3)若板间电场强度E随时间的变化仍如图l所示,磁场的变化改为如图3所示,试画出粒子在板间运动的轨迹图(不必写计算过程)。
解法一:(1)设粒子在o~to时间内运动的位移大小为s1
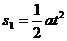 ①
① 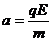 ② 又已知
② 又已知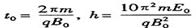
联立①②式解得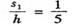 ③
③
(2)粒子在to~2to时间内只受洛伦兹力作用.且速度与磁场方向垂直,所以粒子做匀速圆周运动。设运动速度大小为v1,,轨道半径为R1,周期为T,则
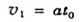 ④
④ 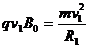 ⑤
⑤
联立④⑤式得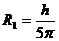 ⑥又
⑥又 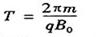 ⑦ R r。鬻⑦
⑦ R r。鬻⑦
即粒子在t。~2to时间内恰好完成一个周期的圆周运动。在2t。~3to时间内,粒子做初速度为v1的匀加速直线运动,设位移大小为s2
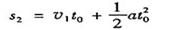 ⑧
⑧
解得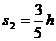 ⑨
⑨
由于s1+s2<h,所以粒子在3to~4to时间内继续做匀速圆周运动,设速度大
小为v2,半径为R2
v2=v1+at0⑩
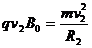
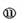
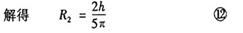
由于s1+s2十R2<h,粒子恰好又完成一个周期的圆周运动。在4t。~5t。时间内,粒子运动到正极板(如图l所示)。因此粒子运动的最大半径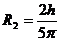 。
。
(3)粒子在板间运动的轨迹如图2所示。
解法二:由题意可知,电磁场的周期为2t0,前半周期粒子受电场作用做匀加速直线运动.加速度大小为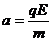 方向向上
方向向上
后半周期粒子受磁场作用做匀速圆周运动,周期为T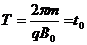
粒子恰好完成一次匀速圆周运动。至第n个周期末,粒子位移大小为sn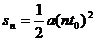
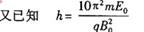
由以上各式得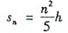
粒子速度大小为 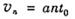
粒子做圆周运动的半径为 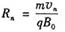
解得 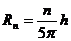
显然s2+R2<h<s3
(1)粒子在0~t0时间内的位移大小与极板间距h的比值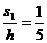
(2)粒子在极板闻做圆周运动的最大半径 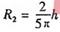
(3)粒子在板间运动的轨迹图见解法一中的图2。
26(19分)番茄(2n=24)的正常植株(A)对矮生植株(a)为显性,红果(B)对黄果(b)为显性,
两对基因独立遗传。请回答下列问题
(1)现有基因型AaBB与aaBb的番茄杂交,其后代的基因型有____种。________基因型
的植株自交产生的矮生黄果植株比例最高.自交后代的表现型及比例为______。
(2)在 AA×
AA× aa杂交中,若A基因所在的同源染色体在减数第一次分裂时不分离.产生的
aa杂交中,若A基因所在的同源染色体在减数第一次分裂时不分离.产生的
雌配于染色体数目为_________,这种情况下杂交后代的株高表现型可能是________。
(3)假设两种纯合突变体X和Y都是由控制株高的A基因突变产生的,检测突变基因转录
的mRNA.发现x的第二个密码子中第二碱基由C变为u,Y在第二个密码子的第二碱
基前多了个U。与正常植株相比,__________突变体的株高变化可能更大,试从蛋白质
水平分析原因:______________.
(4)转基因技术可以使某基因在植物体内过量表达.也可以抑制某基因表达。假设A基因通过控制赤霉素的合成来控制番茄的株高,请完成如下实验设计,以验证假设是否成立。
④实验设计(借助转基因技术,但不要求转基因的具体步骤)
a分别测定正常与矮生植株的赤霉索含量和株高。
b____________________________。
c____________________________。
②支持上述假设的预期结果:____________________.·
③若假设成立,据此说明基因控制性状的方式___________________。
(l)4aaBb矮生红果:矮生黄果=3:1
(2)13或11正常或矮生
(3) YY突变体的蛋白质中氡基酸的改变比x突变体可能更多(或:x突变体的蛋白质可能只有一个氨基酸发生改变,Y突变体的蛋白质氨基酸序列可能从第一个氪基酸后都改变)。
(4)①答案一:
b.通过转基因技术,一是抑制正常植株A基因的表达,二是使A基固在矮生植株过量表达。
c.测定两个实验组植株的赤霉素含量和株高。
答案二
b.通过转基因技术,抑制正常植株A基因的表达,测定其赤霉素含量和株高。
c .通过转基因技术,使A
(答案二中b和c次序不做要求)
②与对照比较.正常植株在A基因表达被抑制后,赤霉素含量降低,株高降低;与对照比较,A基因在矮生植株中过量表达后,该植株赤霉索含量增加,株高增加。
③基因通过控制酶的合成来控制代谢途径,进而控制生物性状。
27(14分)每年的7月11日被定为“世界人口R”,人口问题越来越受到国际社会的重视。下图表示三种可能的人口增长曲线,请回答:
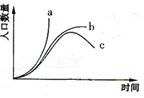
(1)16世纪以来,世界人口增长表现为图中a曲线,人口剧增带来的严重后果有____。如果这种现状不能得到有效改善,人口增长趋势终将表现为图中________曲线。
(2)按生态学原理,世界人口增长应该表现为图中__________曲线,该曲线与a曲线产生差别的原因是_________。若地球环境对人类种群的容纳量(K)为110亿.则全球人口的最适数量为__________。
(3)为缓解人口增长带来的世界性粮食紧张状况,人类可以适当改变膳食结构。若将(草食)动物性与植物性食物的比例由1:1调整为1:4,地球可供养的人口数量是原来的__________倍。(能量传递效率按l0%计算,结果精确到小数点后两位数字)
(4)我国现阶段实行计划生育政策,提倡晚婚晚育,一对夫妇只生一个孩子。这一政策能有效地控制人口增长过快的趋势,原因是__________。
(1)环境污染(环境破坏、生态破坏)、资源短缺(生物多样性降低、可耕地减少)
(2)b环境阻力(资源或空间有限)55亿
(3)1.96
(4)延长世代长度(延长繁衍一代的时间),减少新生儿个体数,降低人口出生率。
28(14分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1) 冶炼铜的反应为
8 CuFeS2+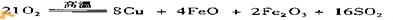
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是__________(填元素符号)。
(2) 上述冶炼过程产生大量SO2。下列处理方案中合理的是________(填代号)
a 高空排放
b用于制备硫酸
c用纯碱溶液吸收制Na2S03,
d用浓硫酸吸收
(3)过二硫酸钾(K2S208)具有强氧化性.可将I-氧化为I2:S2032-十2I-=2SO42-+I2:
通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程._______________________________(不必配平)
(3) 利用黄铜矿冶炼铜产生的炉渣(含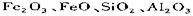 )可制备
)可制备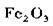 。方法为①用稀盐酸浸取炉渣,过滤。②滤液先氧化,在加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得
。方法为①用稀盐酸浸取炉渣,过滤。②滤液先氧化,在加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得 据以上信息回答下列问题:
据以上信息回答下列问题:
a. 除去Al3+的离子方程式是__________________。’
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
所选试剂为_______________。
证明炉渣中含有FeO的实验现象为__________
(1)Cu、O
(2)b、c
(3)2Fe3++2I-=2Fe2+ +I2 S2082-+Fe2+=2SO42-+2Fe3+
(离子方程式不配平不扣分)
(4)a.Al3++4OH-=AlO2-+2H2O[或Al3++40H-=Al(OH)-
b.稀硫酸 、KMnO4溶液
稀硫酸浸取炉渣所得溶液使KMn04溶液褪色
29(12分)北京奥运会“祥云”火炬燃料是阿烷(C3H8),亚特兰大奥运会火炬燃料是丙烯 (C3H6)。
(1)丙炕脱氢可得丙烯.、
已知C3H8(g)=CH4(g)+HC=CH(g)+H2(g)△H1=156.6 kJ.mol-1。
CH3CH=CH2(g)= CH4(g)+HC=CH(g)△H2=32.4 kJ.mol-1
则相同条件下,反应C3H8(g)= CH3CH=CH2(g) +H2(g)的△H=___________ kJ.mol-1。
(2)以丙烷为燃料制作的新型燃料电池。电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程程式为__________;放电时,C032-移向电池的________(填“正”或“负”)极。
(3)碳氢化台物完全燃烧生成CO2和H20。常温常压下,空气中的CO2溶于水.达到平衡时,溶液的pH=5.60,c(H2CO3)=l.5×10-5mol. L-1.若忽略水的电离及H2CO3的第二级电离,则H2CO3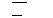 HC03+H+的平衡常数K1=__________(已知10-5.60=2.5×10-6)
HC03+H+的平衡常数K1=__________(已知10-5.60=2.5×10-6)
4)常温下,0.1 mol L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3)______c(CO32-)(填“>”、“=”或“<”),原因是________(用离子方程式和必要的文字说明)。
l)124.2
2)C3H8十502=3C02+4H20负
3)4.2×10-7mol. L-1
4))HCO3-+H2O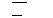 CO32-+H30+(或HCO3-CO32-+H+)
CO32-+H30+(或HCO3-CO32-+H+)
HC03-+H20 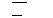 H2CO3-+OH- 、HCO3-的水解程度大于电离程度
H2CO3-+OH- 、HCO3-的水解程度大于电离程度
30(16分)食盐是日常生活的必需品,也是重要的化工原料。
(1) 粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCL的流程如下:
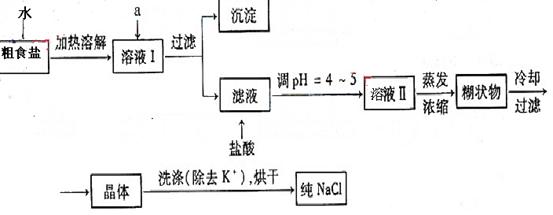
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液NaOH溶液BaCl2溶液 Ba(NO3)2溶液75%乙醇 四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂.按滴加顺序依次为_________________(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_____________
2)用提纯的NaCl配制500 mL4.00 mol. L-1。NaCl溶液,所用仪器除药匙、玻璃棒外还有__________________(填仪器名称)。
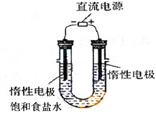
3)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2___________(填“>”、“=”或“<’)2 L,原因是________。装置改进后,可用于制备NaoH溶液,若测定溶液中NaOH的浓度,常用的方法为_________。
4)实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4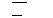 ZnS04+H2↑
ZnS04+H2↑
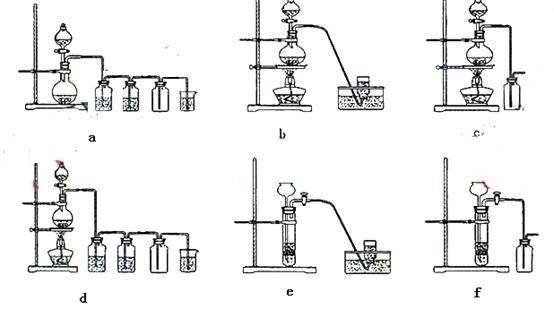
Mn02+4HCl(浓) 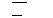 MnCl2+C12↑ +2H20
MnCl2+C12↑ +2H20
据此,从下列所给仪器装置中选择制备并收集H2的装置_______________(填代号)和制备并收集干燥、纯净Cl2的装置______________(填代号)。
可选用制备气体的装置:
(1)①BaCl2、Na0H(1)①BaCl2、NaOH、Na2C03(错选或多选本小题不得分。NaOH溶液的加入顺序及是否答Na0H不影响得分)
②75%乙醇
(2)天平、烧杯、500mL容量瓶、胶头滴管
(3)<电解生成的氯气与电解生成的NaOH发生了反应
酸碱中和滴定
(4)cd
【选做部分】
共8个题,考生必须从中选择2个物理题、1个化学题和1个生物题在答题卡规定的区域作答。
3l(8分)【化学化学与技术】
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在__________部分发生反应,在__________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为_________;加入硅、锰和铝的目的是_________。
(3)不锈钢含有的Cr元索是在炼钢过程的氧吹_________(填“前”或“后”)加入,原因是 _______________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_________。
(1)炉身炉腰
(2)2P+5FeO+3Ca0  Ca3(P04)2+5Fe
Ca3(P04)2+5Fe
脱氧和调整钢的成分
(3)后避免Cr被氧化(或“氧吹前加入Cr会形成炉渣被除去”)
(4)C0燃料(或还原剂)
32(8分)【化学一物质结构与性质】
氢是地球上极为丰富的元素。
(1)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为___________.
(2) N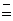 N的键能为942 kJ.mol-1,N-N单键的键能为247kJ.mol-1,计算说明N2中的___________键比____________键稳定(填“σ”或“π”)。
N的键能为942 kJ.mol-1,N-N单键的键能为247kJ.mol-1,计算说明N2中的___________键比____________键稳定(填“σ”或“π”)。
3)(CH3)3NH+和AlCl-可形成离子液体。离子液体由阴、阳离子组成,熔点低于1000C,其挥发性一般比有机溶剂__________(填“大”或“小”).可用作__________(填代号)。
a 助燃剂
b“绿色”溶剂
c复合材料
d绝热材料
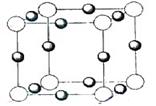
4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是_____________,与同一个N3-相连的X+有__________个。
(1)1s22s22p6
(2)π σ
(3)小 b
(4)Cu6
(8分)【化学一有机化学基础】
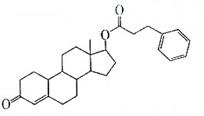
苯丙酸诺龙是一种兴奋剂,结构简式为
(1)由苯雨酸诺龙的结构推测,它能__________(填代号)。
a使溴的四氯化碳溶液褪色b使酸性KMnO4溶液褪色
c.与银氨溶液发生银镜反应 d与Na2CO3溶液作用生成CO2
苯丙酸诺龙的一种同分异构体A,在一定条件下可发生下列反应:
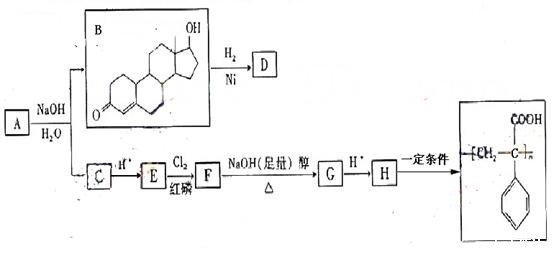
提示:已知反应
据以上信息回答(2)~(4)题:
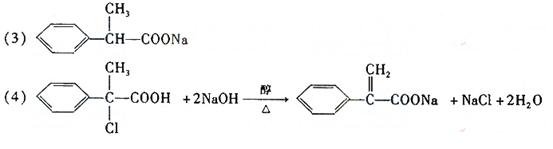
(2)B→D的反应类型是________________。
(3)C的结构简式为__________。
(4)F→G的化学方程式是______________。
(1) a、b
(2)加成反应(或还原反应)
34(8分)【生物一生物技术实践】
科学家发现家蝇体内存在一种抗菌活性蛋白。这种蛋白质具有极强的抗苗能力,受到研究者重视。
(1)分离该抗苗蛋白可用电泳法,其原理是根据蛋白质分子的__________、大小及形状不同,在电场中的___________不同而实现分离。
(2)可用金黄色葡萄球菌来检验该蛋白的体外抗菌特性。抗菌实验所用培养基中的牛肉膏和蛋白胨主要为细菌生长提供_______和____________。
(3)分别在加入和未加入该抗菌蛋白的培养基中接种等量菌液。培养一定时间后,比较两种培养基中菌落的_________,确定该蛋白质的抗菌效果。
(4)细菌培养常用的接种方法有__________和_________。实验结束后,对使用过的培养基应进
行___________处理。
(1)电荷(带电情况)迁移速度
(2)碳源氮源
(3)数量
(4)平板划线法稀释涂布平板法(稀释混合平板法)灭菌
35(8分)【生物一现代生物科技专题】
 为扩大可耕地面积,增加粮食产量,黄河三角洲等盐碱地的开发利用备受关注。我国科学家应用耐盐基因培育出了耐盐水稻新品系。
为扩大可耕地面积,增加粮食产量,黄河三角洲等盐碱地的开发利用备受关注。我国科学家应用耐盐基因培育出了耐盐水稻新品系。
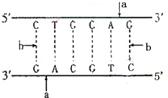
(1)获得耐盐基因后,构建重组DNA分子所用的限制性内切酶作用于图中的__________处,DNA连接酶作用于____________处。(填“a”或“b”)
(2)将重组DNA分子导入水稻受体细胞的常用方法有农杆菌转化法和________法。
(3)由导入目的基因的水稻细胞培养成植株需要利用_________技术,该技术的核心是________和__________。
(4)为了确定耐盐转基因水稻是否培育成功,既要用放射性同位素标记的________作探针进行分子杂交检测.又要用__________方法从个体水平鉴定水稻植株的耐盐性。
(1)aa
(2)基因枪法(花粉管通道法)
(3)植物组织培养(1分)脱分化(去分化)再分化
(4)耐盐基因(目的基因)一定浓度盐水浇灌(移栽到盐碱地中)
36(B分)【物理一物理3—3】
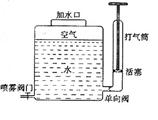
喷雾器内有lOL水,上部封闭有latm的空气2L。关闭喷雾阀门,用打气筒向喷雾器内再充入1 atm的空气3L(设外界环境温度一定,空气可看作理想气体)。
(1)当水面上方气体温度与外界温度相等时.求气体压强,并从微观上解释气体压强变化的原因。
(2)打开喷雾阀门,喷雾过程中封闭气体可以看成等温膨胀,此过程气体是吸热还是放热?简要说明理由。
解:(1)设气体初态压强为P1,体积为V1;末态压强为P2:,体积为V2.由玻意耳定律P1V1=P2V2①
代人数据得P2=2.5 atm②
微观解释:温度不变,分子平均动能不变,单位体积内分子数增加,所以压强增加。
(2)吸热。气体对外做功而内能不变根据热力学第一定律可知气体吸热。
37(8分)【物理一物理3-4】
麦克斯韦在1865年发表的《电磁场的动力学理论》一文中揭示丁电、磁现象与光的内在
联系及统一性,即光是电磁波。
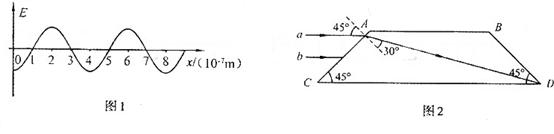
(1)一单色光波在折射率为l.5的介质中传播,某时刻电场横波图象如图1所示,求该光波的频率。
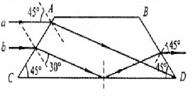
(2)图2表示两面平行玻璃砖的截面图,一束平行于CD边的单色光入射到AC界面上.a、b 是其中的两条平行光线。光线a在玻璃砖中的光路已给出。画出光线b从玻璃砖中首次出射的光路图,并标出出射光线与界面法线夹角的度数。
解:(1)设光在介质中的传播速度为v,波长为 λ,频率为f,则
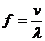 ①
①
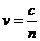 ②
②
联立①②式得 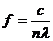 ③
③
从波形图上读出渡长λ4 ×10-7m,代入数据解得
f=5×l014 Hz ④
2)光路如图所示
38(8分)【物理-物理3-5】
(1)在氢原子光谱中,电子从较高能级跃迁到n=2能级发出的谱线属于巴耳末线系。若一群氢原于自发跃迁时发出的谱线中只有2条属于巴耳末线系,则这群氢原子自发跃迁时最多可发出____________条不同频率的谱线。
(2)一个物体静置于光滑水平面上,外面扣一质量为M的盒子,如图1所示。现给盒子一初速度v0,此后,盒子运动的v-t图象呈周期性变化,如图2所示。请据此求盒内物体的质量

解:(1)6
(2)设物体的质量为m.t0时刻受盒子碰撞获得速度v,根据动量守恒定律
Mv0=mv①
3t0时刻物体与盒子右壁碰撞使盒子速度又变为v0,说明碰撞是弹性碰撞
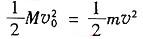 ②
②
联立①② 解得
m=M③
(也可通过图象分析得出v0=v,结合动量守恒,得出正确结果)


