(单词翻译:单击)
第I卷
选择题部分(化学不分有8小题,每题 只有1个正确选项,每题2分,共计16分)
只有1个正确选项,每题2分,共计16分)
8.下列物质中,属于纯净物的是:
A.洁净的空气B.透明的汽水C.固态氧D.NaCl溶液
9.在化学反应中,一定发生变化的是:
A.原子种类B.分子种类C.元素种类D.物质的状态
10.误食工业用盐亚硝酸钠(NaNO2)会使人中毒。NaNO2中氮元素的化合价为:
A.+2B.+3C.+4D.+5
11.李飞同学记录的下列实验数据中,不合理的是:
A.用pH试纸测得某溶液的pH为5.3
B.用10ml的量筒量取7.5ml水
C.测得某粗盐中NaCl的质量分数为92.58%
D.用托盘天平称得食盐16.8g
12.向氢氧化钙的饱和溶液中加入下列物质,不可能使溶液的pH有明显改变的是:
A.通入CO2B.加入稀H2 SO4 C.加入盐酸 D.加入Na2CO3溶液
SO4 C.加入盐酸 D.加入Na2CO3溶液
13.只用一种试剂就可将FeCl3、Na2CO3、MgSO4三种物质的溶液鉴别出来,这种试剂是:
A.AgNO3溶液B.BaCl2溶液C.Ba(OH)2溶液 D.NaOH溶液
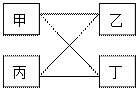
14.下表提供的四组物质中,符合图示相连的两种物质间在一定条件下可以发生化学反应的是:
甲 | 乙 | 丙 | 丁 | |
A | CO | O2 | H2SO4 | Fe2O3 |
B | Zn | HCl | CuSO4 | NaOH |
C | NaOH | SO3 | KOH | CuSO4 |
D | Na2CO3 | Ca(OH)2 | HCl | BaCl2 |
15.相同质量的H2、CH4和CO分别完全燃烧需要氧气的质量:
A.CO最多,H2最少 B.H2最多,CH4最少
C.H2最多,CO最少 D.CH4最多,CO最少
第II卷(非选择题)
(化学部分共有6题)
35 .(3分)已知某粒子(原子或离子)的核外共有2个电子层,其结构示意图为:
.(3分)已知某粒子(原子或离子)的核外共有2个电子层,其结构示意图为:
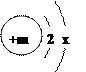
(1)若该粒子为原子时,则m=;
(2)若该粒子为阴离子时,则m-2x(选填“>”“<”或“=”);
(3)若x=8,请写出符合该组成结构且显不同电性的各一种粒子的化学符号:。
36.(4分)如图所示为A、B、C三种物质的溶解度曲线。
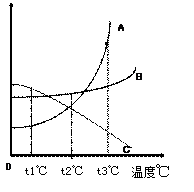
(1)t1℃时,A、B、C三种物质的溶解度大小依次为S1g、S2g、S3g。则S1、S2、S3这三个数中最大的是
,最小的是 ;
(2 )t2℃时,A的溶解度为Sg,该温度下,A的饱和溶液中,溶质的质量分数为 ;
)t2℃时,A的溶解度为Sg,该温度下,A的饱和溶液中,溶质的质量分数为 ;
(3)将t3 ℃时等质量的A、B、C三种物质的饱和溶液降温至t2℃时,所得溶液中溶质的质量分数依次为a%、b%、c%,则a、b、c由大到小的顺序是 。
℃时等质量的A、B、C三种物质的饱和溶液降温至t2℃时,所得溶液中溶质的质量分数依次为a%、b%、c%,则a、b、c由大到小的顺序是 。
37.(7分)已知A、B、C、D、E、F是初中化学中常见的六种物质,它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“”表示两种溶液间能发生反应)。又知A、B、D都是由两种元素组成,且A、B所含元素各不相同;C、E均含三种元素,其中E常用来改良酸性土壤;F是一种能维持生命活动的单质(通常状态下为气体)。请按要求回答下列问题:
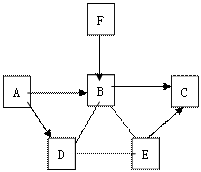
(1)写出F的名称,E的俗名 ;A的化学式;
(2)写出下列反应的化学方程式:
①B---D:
②能生成C,且反应物为两种盐的复分解反应:;
(3)A→D可以通过A分别与 种不同类型的物质反应来实现;
(4)与B组成元素相同的另一种物质的还原性在工业上有重要用途,请写出一个化学方程式予以表示。
38.(4分)用湿润的pH试纸测定某稀盐酸的酸碱度时,若各项操作方法都正确,则所测得的pH比稀盐酸的实际pH (选填“偏大”、“偏小”、或“无影响”)。小明同学用托盘天平称量5.8gNaCl(1g以下用游码)时,若药品放在了右盘,则他所称NaCl的实际值量为g。向一张洁白的滤纸上喷A时,无明显变化;再喷足量的B时,出现了一个红色的小猫图像;接着喷C时,小猫的图像又消失了。已知A、B、C都是实验室常用的试剂。请推测滤纸上原先绘制小猫图像的试剂是 ,A显性(选填“酸”、“碱”或“中”)。
39.(6分)下图是某课外活动小组的同学设计的实验室 制取CO2并检验其性质的装置示意图,请回答下列问题:
制取CO2并检验其性质的装置示意图,请回答下列问题:
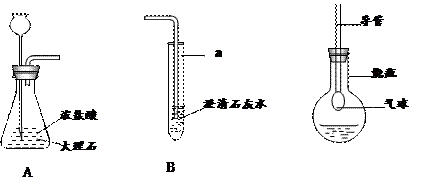
(1)代号a所指仪器的名称是,A装置中发生的化学方程式为;
(2)将A中产生的气体通入到B中一会儿,未见其中变浑浊。李祥同学认为这是浓盐酸挥发出的HCl气体干扰所致。他用 化学方程式表示为:
化学方程式表示为:
Ca(OH)2 + CO2 = CaCO3 ↓+ H2OCaCO3 + 2HCl = CaCl2 + H2O + CO2↑
你的解释还可更简捷,请用一个化学方程式表示:;
(3)张华同学用烧瓶收集A中产生的气体后,向其中加入过量无色透明的M溶液组成C装置,振荡,发现烧瓶中的气球逐渐变大,且溶液始终无色透明,则M可能是 (填写一种物质的化学式);
(4)请设计一个方案,验证C装置中反应的生成物中含有CO32-。简述实验过程:
;
(5)将A中药品换成过氧化氢溶液和二氧化锰。则反应的化学方程式为 。
40.(5分)随机取一定量的镁 粉和铜粉的混合物于烧杯中,再向其中分次加入等质量的同一稀硫酸。实验过程中有关物质的用量及质量测定记
粉和铜粉的混合物于烧杯中,再向其中分次加入等质量的同一稀硫酸。实验过程中有关物质的用量及质量测定记 录如下表:
录如下表:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量 | 35g | 35g | 35g | 35g |
剩余固体的质量 | 8.6g | 7.4g | 6.2g | 5.6g |
请回答下列问题:
(1)随机所取镁粉和铜粉混合物的质量为 g;
(2)实验操作结束后的溶液中溶质的 化学式为 ;
化学式为 ;
(3)所用稀硫酸中溶质的质量分数为 ;
(4)反应后所得溶液的总质量是多少(要有解答过程,结果精确到0.01g)?
参考答案
选择题:
题号 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
答 | C | B | B | A | D | D | C | C |
35.(1)2+x (2)<(3)Na+(或Mg2+等)、O2-(或F-等)
36.(1)S3S1 (2)Sg/(100g+Sg)╳100%(或其他合理表述)(3)b>a>c
37.(1)氧气(写化学式不给分)熟石灰(或消石灰)HCl(写名称不得分)
(2)①CO2  + H2O = H2CO3② Na2CO3 + CaCl2 = CaCO3↓ + 2NaCl (答案不唯一)
+ H2O = H2CO3② Na2CO3 + CaCl2 = CaCO3↓ + 2NaCl (答案不唯一)
(3)三(或其他合理表述)(4)CO+ CuO △ Cu + CO2(答案不唯一)
38.偏大 4.2酚酞溶液  酸或中
酸或中
39.(1)试管 CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
(2)2HCl + Ca(OH)2 = CaCl2 + 2H2O(3)KOH(或NaOH)
(4)向其中加入BaCl2溶液,若生成白色沉淀,即可证明其中含CO32-
(或:向其中加入过量(或足量)的稀盐酸,若有气泡冒出,则可证 明其中含CO32-
明其中含CO32-
(或其他合理表述)(5)2H2O2MnO22H2O+O2↑
40.(1)9.8(2)MgSO4、H2SO4(3)14 % (4)143.85g
% (4)143.85g


