(单词翻译:单击)
一、选择题(每小题只有一个选项符合题意。请将该选项的序号填入题后括号内。每小题2分,共34分)
1.没有蛋白质就没有生命。下列食品中富含蛋白质的是 ( )
A .萝卜 B.香蕉 C.馒头 D.豆腐
.萝卜 B.香蕉 C.馒头 D.豆腐
2.烧碱既是重要的化工原料,又是实验室常用的化学试剂,其化学式为 ( )
A.Na2CO3 B.NaOH C.CaO D.Ca(OH)2
3.下列变化属于物理变化的是 ( )
A.水的蒸发 B.铁钉生锈 C.木炭燃烧 D.指示剂变色
4.下列气体中,既有可燃性又有还原性的是 ( )
A.CO B.O2 C.N2 D.He
5.地壳中含量最多的元素是 ( )
A.O B.Si C.Fe D.Al
6.下列物质性质的表述中,属于化学性质的是 ( )
A.浓硫酸有腐蚀性 B.金属铜能导电 C.蔗糖易溶于水 D.甲烷气体无色无味
7.下列实验操作正确的是 ( )
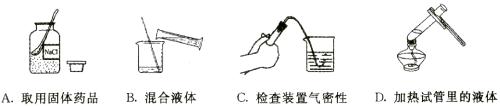
8.有X、Y、Z三种金属,将X、Y浸入稀盐酸中,Y表面有气泡、X无明显现象;将X浸入Z的硫酸盐溶液中,X的表面附着Z金属,则三种金属活动性由强到弱的顺序为 ( )
A.Z、Y、X B.Y、Z、X C.Z、X、Y D. Y、X、Z
9.下列物质分类中错误的一组是 ( )
A.单质 Fe、 S、 N2
B.氧化物 H2O、 P2O5、 Al2O3
C.酸 HCl、 H2SO4、 NH4H2PO4
D.碱 KOH、 Mg(OH)2、 Fe(OH)3
10.科学探究常用到推理的方法,根据下列实验事实推出的结论正确的是 ( )
编号 | 实验事实 | 实验结论 |
A | 某物质常温下是固体 | 该物质一定是晶体 |
B | 某物质可以导电 | 该物质一定是金属单质 |
C | 某反应有二氧化锰生成 | 该反应中二氧化锰一定是催化剂 |
D | 某溶液与碘在一起显蓝色 | 该溶液中一定含有淀粉 |
11.对于图示的理解错误的是  ( )
( )
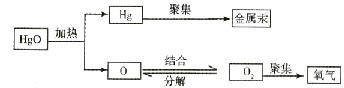
A.原子可以构成物质
B.分子可以构成物质
C.离子不能构成物质
D.可用○+○→○○表示氧分子的形成过程
12.使用右图装置能完成的实验是 ( )
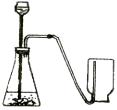
A.高锰酸钾制取收集氧气
B.锌和稀硫酸制取收集氢气
C.大理石和稀盐酸制取收集二氧化碳
D.过氧化氢溶液和二氧化锰制取收集氧气
13.下列有关Fe2O3的反应中,属于置换反应的是 ( )
A. Fe2O3+6HCl=2FeCl3+3H2O
B.Fe2O3十3CO 高温 2Fe+3CO2
C.Fe2O3+2A1 高温 Al2O3+2Fe
D.Fe2O3+3H2SO4=Fe2 (SO4)3+3H2O
14.在①干燥气体、②做反应容器、③与量筒组合测气体体积中,可用下图装置进行操作的是 ( )

A.只有①② B.只有②③
C.只有①③ D.①②③
15.下列试剂:①pH试纸、②无色酚酞溶液、③紫色石蕊溶液、④碳酸钠溶液,其中能将稀盐酸、氯化钠溶液和澄清石灰水鉴别出来的是 ( )
A.①②③ B.①③④ C.②③④ D.①②④
16.已知明矾的化学式为KAl(SO4)2·12H2O,它在水中 能全部解离成K+、Al3+和SO42-,小明同学为了探索明矾的净水原理,将浑浊的天然水分别装入试管①、②、③、④中,做了如下实验:
能全部解离成K+、Al3+和SO42-,小明同学为了探索明矾的净水原理,将浑浊的天然水分别装入试管①、②、③、④中,做了如下实验:
实验操作 | 实验现象 |
①中加入少量明矾,搅拌静置 | 天然水变澄清 |
②中加入少量硫酸铝,搅拌静置 | 天然水变澄清 |
③中如入少量硫酸钾,搅拌静置 | 天然水仍浑浊 |
④中加入少量氯化铝,搅拌静置 | 天然水变澄清 |
由此可知与净水作用关系最大的离子是
A.K+ B.Al3+ C.SO4 2- D.Cl-
17.归纳与比较是学习化学的重要方法,下列有关FeCl2和FeCl3。的知识归纳不正确的是 ( )
A.组成:都是由铁元素和氯元素组成
B.性质:都与氢氧化钠溶液反应生成沉淀
C.制取:都可以用铁和稀盐酸反应来制取
D.分类:都属于盐类
得分 | 评卷人 |
二、填空题(共26分)
18.(4分)请描述下列实验现象。
(1)铁丝在氧气中燃烧:_______________________ _________________________。
_________________________。
(2)向过氧化氢溶液中加入少量二氧化锰:________________________________。
(3)向硫酸铜溶液中加入铝片:__________________________________________。
(4)向氯化钠溶液中滴加硝酸银溶液:____________________________________。
品名 休闲牛仔裤 型号 175/86A 面料 棉 74.3% 涤纶25.7% |
批号 X001 |
19.(8分)生活中处处有化学,按要求完成下列各题。
(1)某服装标签如右图,该服装面料含有的天然纤维是________,合成纤维是____________,鉴别天然纤维和合成纤维的方法是
______________________________________。
(2)膳食合理,营养均衡是健康的基本保证。食品营养素中,可以调节体内许多代谢反应的有机营养索是_________________________________。
(3)新装修的房屋常 闻到装修材料中释放出的刺激性气味,人们能闻到这种气味的原因是分子______________________________________。
闻到装修材料中释放出的刺激性气味,人们能闻到这种气味的原因是分子______________________________________。
(4)自行车是很多人出行的工具,写出一条防止自行车链条生锈的措施____________
__________ _______________________________。
_______________________________。
(5)“84消毒液”常用于家庭、医院、车站等扬所的消毒,其主要成分是次氯酸钠。次氯酸钠由钠、氯、氧三种元素组成,其中氯显+1价。则次氯酸钠的化学式为___
_________。
20.(9分)下图中的①、②分别是氯元素、钠元素在周期表中的信息,A、B、C、D是四种粒子结构示意图。
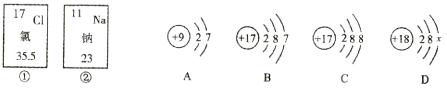
请你回答下列问题:
(1)钠元素的原子序数为_______,画出它的原子结构示意图___________;氯元素的相对原子质量为___________。
(2)示意图D中的χ=________。
(3)A、B、C、D中属于同种元素的粒子是____和_____(填序号)。
(4)A和B两种粒子的__________相同,所以它们具有相似的化学性质。
(5)钠在氯气中燃烧的化学方程式为:_____________________________________。
21.(5分)下图是甲、乙两种固体物质的溶解度曲线,回答下列问题:
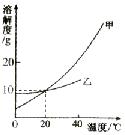
(1) 20℃时,甲物质的溶解度是_______g。
(2)20'C时,甲物质的饱和溶液中,溶质和溶剂的 质量比为__________。
质量比为__________。
(3)将40℃时的乙物质的饱和溶液变为不饱和溶液,可采用的方法是______________(写一种即可)。
(4)40'C时,将甲、乙两物质的饱和溶液分别降温到20'C,所得溶液的溶质质量分数的大小关系是________。
(5)甲的热饱和溶液中含有少量的乙,若提纯甲,可采用______________法(填“冷却结晶”或“蒸发结晶”)。
三、简答题(共12分)
22.(8分)实验室里有稀硫酸、氧化铜、铁粉三种物质,请你设计两种方案制取铜(用化学方程式表示)。
方案一:______________________________________________________________。
方案二:______________________________________________________________。
23.(4分)甲、乙、丙是初中化学常见三种物质,甲、己、丙含有相同的一种元素,且丙是一种气体单质,它们相互转化关系如右圈。
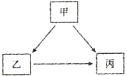
则甲的化学式为___________。甲转化为丙的化学方程式为_______________________。其基本反应类型为_________。
得分 | 评卷人 |
四、 实验与探究题(共1 2分)
实验与探究题(共1 2分)
24.(3分)为了探究溶质在水中溶解速率的影响因素,某学习小组设计了如下实验:
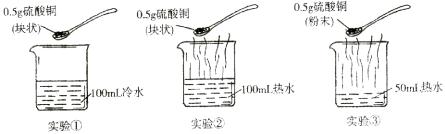
下列说法中正确的是 ( )
A.对比实验①和②,可探究水的温度对溶质在水中溶解速率 的影响。
的影响。
B.对比实验②和③,可探究水的温度对溶质在水中溶解速率的影响。
C.对比实验②和③,可搽究固体溶质的形态对溶质在水中溶解速率的影响。
D.对比实验①和③,可探究固体溶质的形态对溶质在水中溶解速率的影响。
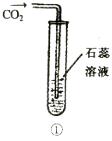
25.(9分)在学完“二氧化碳性质的探究”后,小明同学觉得按照课本实验(图①)不能完全说明是什么物质使紫色石蕊溶液变为红色。他和小娜同学进行了如下实验探究:
【猜想与假设】
 猜想一:水使紫色石蕊溶液变红
猜想一:水使紫色石蕊溶液变红
猜想二:二氧化碳使紫色石蕊溶液变红
猜想三:二氧化碳与水反应生成的新物质使紫色石蕊溶液变红
【查阅资料与实验准备】
(1)将纸条浸泡在紫色石蕊溶液中,晾干后可制得紫色石蕊试纸。
(2)自制的紫色石蕊试纸遇酸变红色,遇碱溶液变蓝色。
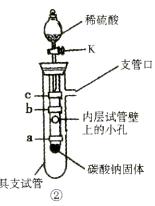
【设计与实验】
小明同学设计了实验装置如图②。
图中b为紫色石蕊试纸,缠绕在小试管上;
a、c为湿润的紫色石蕊试纸,缠绕在小试管上。
(1)通过对比观察图中a、b得出结论:
猜想_________不正确。
(2)打开活塞K,滴人稀硫酸,观察并解释实验现象:
①试纸b没有明显变化,得出结论:猜想_______不正确。
②试纸a、c由紫色变为红色,得出结论:_______________________(用化学方程式表示)猜想________正确。
③试纸______首先变色,其原因是________________________________。
【交流与反思】
小娜同学认为,上图装置还可以同时验证:①二氧化碳能使澄清石灰水变浑浊;
②二氧化碳不能燃烧也不支持燃烧。
为了完成小娜同学的两个验证实验,请你对上面的实验裴置进行简单的改进:
____________________________________、_________________________________。
得分 | 评卷人 |
五、计算题(共6分)
26.(6分)为测定未知浓度稀硫酸的溶质质量分数,取氢氧化钡溶液15g,逐滴加入该待测稀硫酸,同时测定并纪录反应过程中混合溶液的pH变化情况(如下图所示),过滤后得到滤液32. 67g。
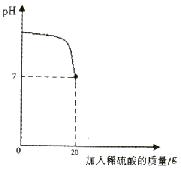
计算:
(1)反应后生成硫酸钡的质量为________g。
(2)求该稀硫酸的溶质质量分数。
可能用到的 资料:
资料:
①相对原子质量:H-1 10-16 S-32 Ba-137
②化学方程式:Ba(OH)2+H2SO4= BaSO4↓+2H2O
2012年赤峰市初中毕业、升学统一考试试卷化学参考答案及主分标准
一、选择题(每小题2分,共34分)
1.D 2.B 3.A 4.A 5.A 6.A 7.C 8.D 9.C 10.D 11.C 12.B 13.C 14.D 15.B 16.B 17.C
二、填空题(共26分)
18.(4分)(1)剧烈燃烧,火星四射 (2)产生大量气泡 (3)铝片表面有红色物质析出 (4)产生白色沉淀
19.(8分)(1)棉 涤纶 抽丝灼烧 (2)维生素 (3)在不断运动 (4)涂油(或防止与水接触等) (5)NaC1O(2分)
20.(9分)(1)11 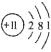 35.5 (2)8
35.5 (2)8  (3)B C (4)最外层电子数
(3)B C (4)最外层电子数
(5)2Na+Cl2 点燃 2NaCl(2分)
21.(5分)(1)10 (2)1:10 (3)加溶剂(或升高温度) (4)相等 (5)冷却结晶
三、简答题(共12分)
22.(8分)方案一:H2SO4+CuO=CuSO4+H2O Fe+CuSO4=Cu+FeSO4
方案二:Fe+H2SO4 = FeSO4+H2↑ H2十CuO △ Cu+H2O
23.(4分)H2O2 2H2O2 MnO2 2H2O2+O2↑ 分解反应
四、实验与探究题(共12分)
2![]() 4.(3分) A
4.(3分) A
25.(9分)(1)一 (2)①二 ②CO2+H2O=H2CO3(2分)三 ③a 二氧化碳密度比空气密度大。
【交流与反思】在具支试管(或外管、大试管)内装入澄清石灰水、将燃着的火柴放在支管口
五、计算题(共6分)
26.解:(1)生成硫酸钡的质量为:20+15 - 32. 67=2.33g……………(2分)
(2)设生![]() 成2.33gBaSO4需硫酸的质量为x ……………(1分)
成2.33gBaSO4需硫酸的质量为x ……………(1分)
Ba(OH)2+H2SO4 =BaSO4↓+2H2O
98 233
x 2.33g…………………………………(1分)
x=0.98g ……………………………………………(1分)
稀硫酸的溶质质量分数为:0.98g/20g×100%=4.9%………………(1分)
答:稀硫酸的溶质质量分数为4. 9%。
评分说明:
(1)其它正确解法请参照本标准给分。
(2)化学方程式中若化学式书写错误给0分,书写不完整(如缺少状态符号、反应条件,没有用等号连接,未配平等)扣1分。
(3)26题出现所设未知数后加单位,计算过程中已知物质质量、计算结果缺单位,缺少解、设、答等情况扣1分。


