(单词翻译:单击)
卷Ⅰ
一、选择题(每小题4分。请选出一个符合题意的正确选项,不选、多选、错选,均不给分)
1.臭氧(O3)、二氧化氯(ClO2)、双氧水(H2O2)等都是生产、生活中常用的消毒剂,三种物质中都含有
A.氧分子B.氧离子C.氧气 D.氧元素
3.CeCu2Si2是一种高温超导材料。CeCu2Si2中铜元素的化合价为+2价,硅元素的化合价为-4价,则铈(Ce)元素的 化合价为
化合价为
A.一4B.一2C.+2D.+4
7.当一位科学家通过实验宣称在某领域获得一项重要发现时,判断这项发现是否可信的最好理由是
A.该领域其他专家的意见B.实验报告撰写的详细程度
C.该科学家是否为这一领域的权威D.他人能否重复其实验并得到相同的结果
8.同学们在做氧气性质实验时,将点燃的木炭伸人集气瓶内,有的现象明显,有的却不明显。导致现象不明显的原因可能是
A .排水法收集前未将集气瓶灌
.排水法收集前未将集气瓶灌 满水B.导管口连续放出气泡时开始收集氧气
满水B.导管口连续放出气泡时开始收集氧气
C.收集满后盖上毛玻璃片拿出水面D.收集满氧气的集气瓶正放于桌面
10.某科学兴趣小组要在实验室制取一定量的MgSO4。同学们分别在实验室里找到了以下四种反应物,其中 不能通过与稀硫酸反应制得MgSO4的是
不能通过与稀硫酸反应制得MgSO4的是
A.Mg B.MgO
C.Mg(OH)2D.MgCl2
13.往一定量的稀硫酸中加入过量的锌粒,如图是反应过程中某种量Y随加入锌粒的质量变化的关系,则Y不可能表示
A.溶液中水的质量B.生成硫酸锌的质量
C.参加反应的硫酸质量D.生成氢气的质量
17.下列实验设计,不能达到实验目的的是
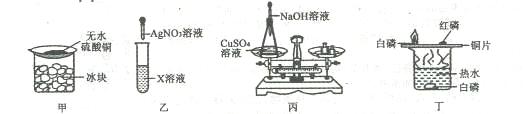
A.甲装置验证空气中有水分B.乙装置验证X溶液中是否含有Cl—
C.丙装置验证质量守恒定律D.丁装置验证可燃物燃烧的两个条件
卷Ⅱ
二、简答题(每空格3分)
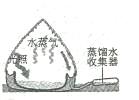
23.生活中有很多物品可以为科学实验所用。如图所示,玻璃瓶中都装满冷开水,并加入碳酸氢钠(一种CO2释放 剂)。将装置置于光照条件下,一段时间后,_______(选填“甲”或“乙”)瓶中的铁钉先出现锈迹,原因是_______。
剂)。将装置置于光照条件下,一段时间后,_______(选填“甲”或“乙”)瓶中的铁钉先出现锈迹,原因是_______。
24.根据事物某一方面的特征,按其异同或有无分为两组,如此反复,可使它们之间的关系变得更加清晰。-
(2)CO2、SO2、MgO、CuO都属于氧化物,若依据组成元素的不同,可将它们分为 _______两类。
28.模型可以反映客观现象,简单明了地表示事物。
(1)某矿石样品中可能含有碳酸钙、二氧化硅、氧化铝、氧化铁等化合物,经测定各元素质量分数的模型如
图甲。由此可推测,该样品中不可能含有的化合物是_______。
(2)图乙是某同学模仿甲图构建的尿素[CO(NH2)2]各元素质量分数的模型,则图中的D表示的是_______元素。

29.根据已知物质和未知物质的特性,运用实验的方法,可以鉴别某些物质。有3包白色粉末,它们分别是碳酸钠、氯化钠、氧化钙中的一种,现用实验 的方法将它们一一区分。
的方法将它们一一区分。
(1)取少量3种粉末,分别装入编号为甲、乙、丙的三支试管中,加水后都能溶解。其中甲试管壁明显变热,由此可知甲试管中加的粉末是__________。
(2)取甲试管中的溶液分别滴入另两支试管中,乙试管中出现白色沉淀,丙试管中无明显现象。请写出乙试管中发生反应的化学方程 式__________。
式__________。
三、实验探究题(每空格2分)
31.为研究实验室制取二氧化碳的速度与什么因素有关, 科学兴趣小组的同学设计了如下实验方案:室温下在六个锥形瓶中分别加入A、B两种大理石各50克 ,然后加入等量的不同溶质质量分数的稀盐酸。记录表如下:
,然后加入等量的不同溶质质量分数的稀盐酸。记录表如下:
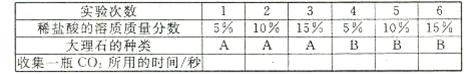
(1)由实验方案可知, 他们除了研究稀盐酸的质量分数会影响CO2的产生速度外,还在研究_____的影响。
他们除了研究稀盐酸的质量分数会影响CO2的产生速度外,还在研究_____的影响。
(2)查阅资料得知,化学反应的速度与反应物间的接触面积有关。于是他们对上述方案进行了修改,使 大理石的 _____也相同。
大理石的 _____也相同。
(3)为了准确比较CO2气体的产生速度,理论上可以测量收集相同体积气体所用的时间,也可以测量_____。
34.氢气还原氧化铜生成红色固体,这 些红色固体是什么物质?某科学兴趣小组查阅资料得知,反应温厦不同,氢气还原氧化铜的产物可能是Ca或Cu2O,Cu和Cu2O均为不溶于水的红色固体;但氧化亚铜能与稀硫酸反应,化学方程式为:Cu2O+H2SO4=Cu SO4+Cu+H2O。
些红色固体是什么物质?某科学兴趣小组查阅资料得知,反应温厦不同,氢气还原氧化铜的产物可能是Ca或Cu2O,Cu和Cu2O均为不溶于水的红色固体;但氧化亚铜能与稀硫酸反应,化学方程式为:Cu2O+H2SO4=Cu SO4+Cu+H2O。
为探究反应后的红色固体中含有什么物质?他们提出了以下假设:
假设一:红色固体只有Cu
假设二:红色固体只有Cu2O
假设三:红色固体中有Cu和Cu2O
请回答有关问题。
(1) 取少量红色固体,加入足量的稀硫酸。若无明显现象,则假设_____成立;若看到溶液变成蓝色 ,且仍有红色固体,则能否支持假设三?_____(选填“能”或“不能”)。
,且仍有红色固体,则能否支持假设三?_____(选填“能”或“不能”)。
(2) 现将3克红色固体加入足量的稀硫酸中,反应后的溶液过滤,称得烘干后的滤渣质量为1.4克,则原红 色固体中含有什么物质?_____。
色固体中含有什么物质?_____。
四、分析计算题
36.如图是某同学在厨房里看到的食用纯碱(主要成分是Na2CO3)包装袋信息,他带了一包食用纯碱到学校实验室。

(1)为测定室温下Na2CO3的溶解度,在编号为A、B、C、D的四个烧杯中各加入室温下的水100g。并 分别加入取自实验室的Na2CO3固体,搅拌至充分溶解。实验数据记录如下表:
分别加入取自实验室的Na2CO3固体,搅拌至充分溶解。实验数据记录如下表:
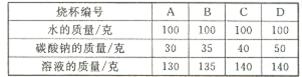
分析上述数据可知,烧杯编号为_________中的溶液是饱和溶液。室温下,Na2CO3的溶解度是_________克。
(2)为确定食用纯碱的纯度,称取自带的食用 纯碱5.4g放人烧杯中,再滴加盐酸至刚好完全反应,共用去
纯碱5.4g放人烧杯中,再滴加盐酸至刚好完全反应,共用去 稀盐酸25g,得溶液质量为28.2g(反应的化学方程式为:2HC
稀盐酸25g,得溶液质量为28.2g(反应的化学方程式为:2HC I+Na2CO3=2NaCI+H2O+CO2↑,杂质溶于水且与盐酸不反应)。通过计算判断该食用纯碱中碳酸钠的质量分数是否与包装信息相符。(计算结果精确到0.1%)
I+Na2CO3=2NaCI+H2O+CO2↑,杂质溶于水且与盐酸不反应)。通过计算判断该食用纯碱中碳酸钠的质量分数是否与包装信息相符。(计算结果精确到0.1%)
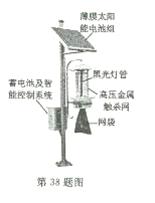
38.如图是一个太阳能黑光灯灭虫装置,上方的薄膜太阳能电池组将太阳能转化成电能,为诱虫的黑光灯及高压金属触杀网供电。
(4)为保护环境,对含镉固体废弃物必须及时处理。下面是处理过程中某一重要反应:
CdSO4+Na2S = CdS↓+ Na2SO4,通过该反应把可溶性的CdSO4转化为不溶性的CdS,以减轻对土壤的污染。该反应的基本类型是_________。
浙江省2013年初中毕业生学业考试(嘉兴卷)
化学参考答案
一、选择题(每小题4分。请选出一个符合题意的正确选项,不选、多选、错选,均不给分)
1.D3.D7.D8.A10.D13.A17.B
二、简答题{每空格3分)
23.甲光合作用产生氧气
24.(2)金属氧化物和非金属氧化物
28.(1)碳酸钙(CaCO3)(2)氧(O)
29.(1) 氧化钙(CaO) (2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
三、实验探究题(每空格2分)
31.
(1)大理石的种类(2)颗粒大小(体积)
(3)相同时间收集到的气 体体积
体体积
34.(1)一 不能 (2)Cu和Cu2O
36.
(1)C、D 40
(2)设纯碱样品中碳酸钠的质量分数为x
CO2的质量=5.4克+25克-28.2 克=2.2克
克=2.2克
Na2CO3+2HCl=2NaCl+H2O+CO2↑
10644
5.4克x 2.2克
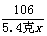 =
=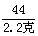 x=98.1%>98% ∴符合。
x=98.1%>98% ∴符合。
答:纯碱样品中碳酸钠的质量分数为98.1%,符 合包装信息。
合包装信息。
38.(4)复分解反应。


